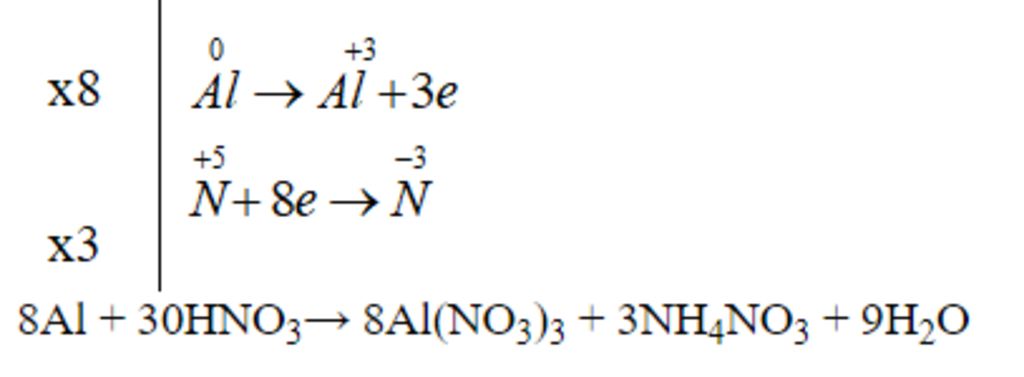Nitơ là một khí không còn xa lạ gì với mỗi chúng ta, nó được ứng dụng rất nhiều trong cuộc sống bởi đặc tính về mặt vật lý và hóa học của nó. Tuy nhiên, để biết được khí nitơ có độc hay không, cùng bài viết này tìm hiểu nhé:
Mục lục bài viết
1. Khái quát về khí Nitơ:
1.1. Khí Nitơ là gì?
Nitơ là một nguyên tố hóa học chiếm khoảng 78% trong không khí hay khí quyển của Trái Đất và là thành phần có trong mọi cơ thể sống (cơ thể con người chứa khoảng 3% nitơ theo trọng lượng).
Khí Nitơ tinh khiết là một chất khí không mùi, không vị, ở dạng phân tử không màu. Là khí trơ chỉ tham gia phản ứng hóa học phản ứng với Liti ở nhiệt độ phòng. Khí Nitơ là thành phần tạo ra nhiều hợp chất quan trọng như axít amin, axit nitric, amoniac và các xyanua trong cơ thể sống.
Nitơ (tên tiếng Anh là nitrogen),
Trong hóa học, Nitơ (từ gốc là Nitro) là một nguyên tố hóa học ở vị trí thứ 7, chu kì 2, thuộc nhóm VA trong bảng tuần hoàn hóa học. Có công thức hóa học là N2 và thường tồn tại ở dạng khí với liên kết 3 có công thức cấu tạo N ≡ N.
Cấu hình electron nguyên tử: 1s2 2s2 2p3. Như vậy, cấu trúc electron của N2 gồm 2 lớp, lớp ngoài cùng vỏ có 5 electron hoạt động. Vì vậy, loại khí này được coi là một phi kim hoạt động mạnh.
1.2. Nitơ có trong không khí không?
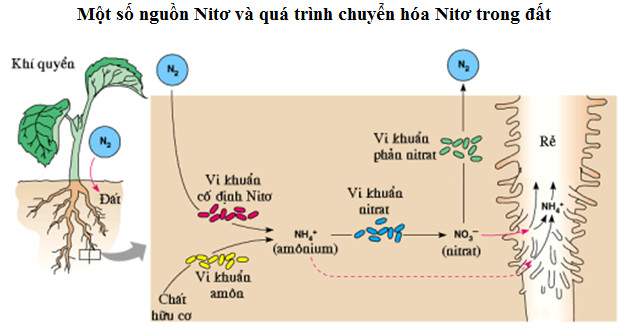
Để trả lời cho câu hỏi Nitơ có trong không khí không, ta cần biết: trong tự nhiên, nitơ tồn tại dưới dạng tự do và hợp chất.
– Trong thiên nhiên, khí Nitơ chiếm 78.16% thể tích không khí, là hỗn hợp của 2 đồng vị: 14/7N(99.63%) và 15/7N(0.37%). Như vậy, khí nitơ chiếm phần lớn thể tích của không khí.
– Nito dưới dạng hợp chất có nhiều trong natri nitrat NaNO3 với tên gọi diêm tiêu natri.
– Nito có mặt cơ thể sống chủ yếu dưới dạng các amino acid (protein) và cũng có trong các acid nucleic (RNA và DNA). Theo nghiên cứu, cơ thể con người chứa khoảng 3% nitơ theo trọng lượng. Đây là nguyên tố phổ biến thứ tư trong cơ thể đứng sau oxy, cacbon và hydro.
1.3. Nitơ có phải khí độc không?
Ở điều kiện bình thường, khí Nitơ không duy trò sự cháy (khác với oxy có duy trì sự cháy), vì vậy mà Nitơ được ứng dụng trong công tác chữa cháy:
– Nitơ có tính dẫn điện thấp nên các bình cứu hỏa chứa khí Nitơ có thể sử dụng dập tắt các đám cháy thiết bị điện.
– Làm giảm nhiệt trong các đám cháy.
– Giảm nồng độ oxi trong vùng cháy.
Mặc dù không duy trì sự sống, không duy trì sự cháy, và với mật độ chiếm gần 80% trong không khí mà không ảnh hưởng đến sức khỏe, cơ thể ta vẫn sống bình thường bỏi hàm lượng oxy vẫn đảm bảo. Có thể thấy rằng khí Nitơ là một khí không có độc. Tuy nhiên, việc sử dụng Nitơ quá cao trong cơ thể có thể gây sốc liệt tay chân.
Bên cạnh đó, các sản phẩm kem hay bánh chế biến từ Nitơ lạnh sẽ lạnh hơn những sản phẩm khác nên nếu sử dụng vội vàng có thể bị bỏng lạnh, nên chờ cho phần khói của sản phẩm tan hết rồi mới dùng để tránh bị thương.
2. Tính chất của khí nitơ:
Tính chất vật lý:
Nitơ là một chất khí không màu, không mùi, không vị và có khối lượng nhẹ hơn không khí N2=28, hay còn gọi là đạm khí.
Nitơ ít tan trong nước ở điều kiện thường (1 lít nước sẽ hòa tan được 0.015 lít khí nitơ).
Nhiệt độ hóa lỏng của Nitơ ở – 196 độ C và nhiệt độ hóa rắn cũng rất thấp. Nitơ lỏng là một dạng hợp chất giống nước nhưng chỉ có 80.8% nitơ ở điểm sôi, hằng số điện môi là 1.4.
Khí Nitơ không duy trì sự cháy và sự sống.
Tính chất hóa học:
Nitơ là một chất có liên kết 3 rất bền, thậm chí ở 3000 độ C nó vẫn chưa bị phân hủy rõ rệt thành các nguyên tử, không phản ứng với các chất khác (có phản ứng với Liti), vì vậy mà Nitơ có tính trơ về mặt hóa học.
Tuy nhiên, Nitơ trở nên hoạt động hơn và tác dụng được với nhiều chất khi ở nhiệt độ cao.
Trong các hợp chất cộng hóa trị của nitơ với những nguyên tố có độ âm điện nhỏ hơn (như hidro, kim loại…), nitơ có oxi hóa -3.
Trong các hợp chất cộng hóa trị của nitơ với những nguyên tố có độ âm điện lớn hơn (oxi, clo, flo), nitơ có số oxi hóa dương, từ +1 đến +5.
Vì vậy, khi tham gia phản ứng oxi hóa – khử, nitơ có thể giảm hoặc tăng số oxi hóa. Vì lý do này, nitơ vừa có tính oxi hóa, vừa có tính khử. Trong đó, tính oxi hóa là tính chất chủ yếu của N2.
3. Ứng dụng của Nitơ:
Với những đặc tính vật lý và hóa học đặc biệt của mình, Nito được ứng dụng rộng rãi trong đời sống và ngày càng trở nên phổ biến. Đặc biệt là nito dạng khí để phục vụ sản xuất nito lỏng.
Nito trong bảo quản thực phẩm:
Vì có đặc tính trơ về mặt phản ứng, nên Nitơ có khả năng ngăn chặn được ảnh hưởng của sự oxy hóa rất tốt, có thể làm chậm sự ôi thiu và các dạng tổn thất khác gây ra bởi oxi hóa. Vì thế nên nito được ứng dụng trong việc bảo quản thực phẩm, được ứng dụng để đóng gói hay dạng rời thực phẩm. Ngoài ra, ngày nay người ta còn sử dụng khí Nitơ hóa lỏng còn được dùng để tạo áp lực cho thùng chứa một số loại bia thay thế cho khí CO2.
Nito trong ứng dụng trong hàn ống, chế biến kim loại:
Nitơ có khả năng làm sạch đường ống đảm bảo an toàn, không hư hại tới các sản phẩm khác nên được rất nhiều người ưa chuộng sử dụng, ap dụng trong việc hàn ống, cũng như chế biến các loại kim loại, nâng cao độ bền chắc chắn hơn cho sản phẩm
Nito ứng dụng để luyện kim và chế tác kim loại:
Với đặc tính hóa học của mình, trong ngành luyện kim hay sản xuất các linh kiện điện tử, sản xuất thép không rỉ thường cần tới sự có mặt của nitơ để hỗ trợ sản xuất. Ở tùy thuộc vào đặc thù của công việc và nhu cầu sử dụng sẽ có kêu lượng và mức độ sử dụng khác nhau.
Nitơ trong việc bơm lốp ô tô và máy bay:
Với đặc tính trơ và thiếu ẩm của mình, đặc biệt oxy hóa cực thấp vì thế chỉ nitơ được sử dụng rất nhiều trong việc bơm lốp ô tô hoặc máy bay.
Khí nitơ trong vận chuyển thực phẩm và các mẫu chế phẩm sinh học:
Tồn tại ở trạng thái tự nhiên có nhiệt độ cực lạnh và đặc tính giúp làm lạnh an toàn mà không gây hại cho thực phẩm. Vì vậy mà khí nitơ được sử dụng trong việc làm lạnh nhằm phục vụ việc vận chuyển thực phẩm, giúp ích cho việc bảo vệ các bộ phận cơ thể cũng như đảm bảo cho các tế bào tinh trùng và trứng được bảo quản.
Nito trong nghiên cứu, giáo dục:
Nitơ là thành phần có trong rất nhiều hợp chất vì vậy cũng được sử dụng trong học phần môn hóa học, được sử dụng trong việc phân tích mẫu, đảm bảo cho quá trình nghiên cứu cũng như truyền đạt kiến thức cho các em học sinh biết đặc tính của một số hợp chất khác.
Trong y tế:
Nitơ giúp bảo quản các bộ phận cơ quan của thân thể, bảo quản máu, các tế bào tinh trùng và trứng, các chế phẩm sinh học. Trong da liễu học để loại bỏ các tổn thương da ác tính xấu xí hay tiềm năng gây ung thư người ta cũng dùng khí Nitơ hóa lỏng. Ví dụ loại bỏ các mụn cóc, các vết chai sần trên da v.v.
Trong công tác chữa cháy:
Nito có tính dẫn điện thấp nên các bình cứu hỏa khí N2 có thể sử dụng dập tắt các đám cháy thiết bị điện, làm giảm nhiệt trong các đám cháy, giảm nồng độ oxi trong vùng cháy.
4. Những tác hại của khí nitơ có thể gây ra:
Mặc dù là thành phần chứa đến 78% trong không khí mà chúng ta đang sống, được ứng dụng rất nhiều trong thực tế và có đặc tính làm lạnh bảo quản thực phẩm an toàn. Nhưng trong quá trình sử dụng không thể tránh khỏi các tai nạn ngoài ý muốn sau:
Gây bỏng lạnh do Nitơ lỏng:
Nitơ lỏng là một dạng hợp chất giống nước nhưng chỉ có 80.8% nitơ ở điểm sôi, hằng số điện môi là 1.4, nhiệt độ hóa lỏng của Nitơ ở – 196 độ C và nhiệt độ hóa rắn cũng rất thấp. Nên trong quá trình sử dụng hay đang chuyển đổi Nitơ từ dạng lỏng sang dạng khác, nếu để da khi chạm vào lâu mà không có biện pháp xử lý kịp thời sẽ bị bỏng lạnh, vết thương có thể bị hoại tử và nặng hơn là tử vong, dính vào mắt có thể gây mù lòa. Trường hợp này thường gặp tại các khu sản xuất, trạm cung cấp và sang chiết nitơ lỏng.
Gây ra tình trạng ngạt thở:
Mặc dù khí nitơ chiếm thể tích lớn trong khí quyển nhưng lại không có đặc tính duy trì sự sống. Môi trường không khí tốt dành cho con người là có 21% oxy, nếu ở mức dưới 19% sẽ gây khó thở. Nếu để Nitơ trong không gian kín hoặc do Nitơ bị hóa khí chiếm hết hàm lượng oxy, khi được sử dụng với nồng độ quá lớn hay hít vào lượng lớn thì sẽ gây ra các tình trạng: khó chịu, buồn nôn, nôn mửa; Người bị nạn cảm giác ngứa ran, ngạt thở, có thể đau thắt ruột; Gây ngạt thở, nguy hiểm hơn nó cũng có thể sẽ gây ra chết người.
Có thể làm nổ thiết bị chứa:
Nitơ được bảo quản trong bình kín. Nếu việc bảo quan không tốt, bình chứa hết niên hạn hoặc chất lượng không tốt, Nitơ lỏng nếu được lưu trữ trong không gian kín và xảy ra tình trạng hóa hơi đột ngột do gia tăng áp suất sẽ gây nổ, ảnh hưởng đến tính mạng những người xung quanh.
Tác động đến các vật liệu tiếp xúc gần:
Nitơ lỏng có nhiệt độ thấp đến -195,8oC nên ngay các vật liệu tiếp xúc gần hay trực tiếp với nitơ lỏng cũng có thể bị biến dạng hay nứt vỡ, biến dạng do chênh lệch nhiệt độ.
Gây tình trạng ô nhiễm môi trường:
Các sản phẩm phân bón có thành phần nitrat khi bị rửa trôi sẽ ngấm vào đất, nguồn nước ngầm và chảy ra các kênh ngòi sông suối gây ra cái chết của nhiều loài sinh vật, ảnh hưởng mạnh đến sức khỏe con người.
5. Biện pháp phòng tránh các nguy hiểm khi sử dụng khí nitơ:
Khi bảo quản:
Yêu cầu khi bảo quản khí Nitơ canaf áp dụng đúng biện pháp và điều kiện, sử dụng bình chứa còn niên hạn, còn chất lượng tốt, các chỉ số thông gió, chỉ dùng trong hệ thống kín, sử dụng các thiết bị điện phòng nổ, vận chuyển nội bộ an toàn,…
Bảo quản đúng cách, đúng nhiệt độ, tránh để trong môi trường kín, tránh bảo quản chung với các nguồn gây cháy, nổ, tách riêng những chất không tương thích.
Khi làm việc:
Cần được đào tạo chuyên nghiệp trước khi làm công việc có liên quan đến Nitơ, khi thao tác với khí nitơ cần có các phương tiện bảo hộ cá nhân an toàn. Sau mỗi lần tiếp xúc cần rửa tay, thay quần áo đã bị ô nhiễm.
Nên chọn mua các bình khí Nitơ tại các địa chỉ tin cậy, đảm bảo an toàn về bình, thùng chứa khí, tránh tối đa các nguy cơ xảy ra sự cố cháy, nổ, rò rỉ.