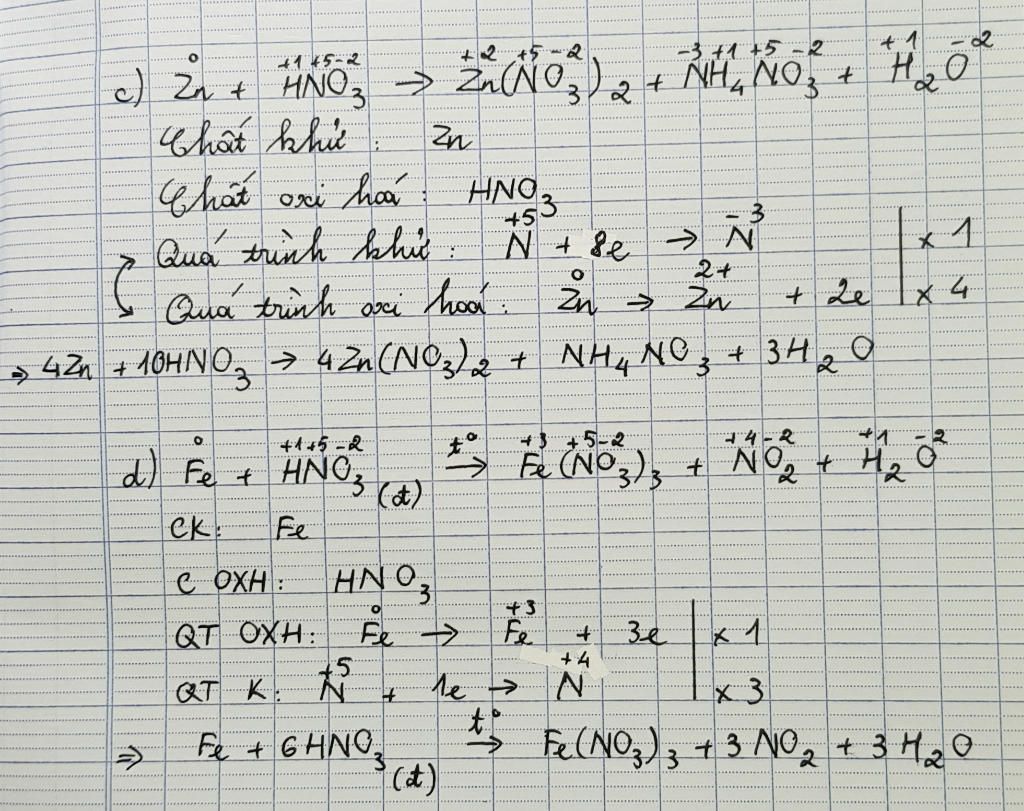Kẽm (Zn) không chỉ là một nguyên tố hoá học quan trọng mà còn là một kim loại có nhiều ứng dụng đa dạng và quan trọng trong nhiều lĩnh vực khác nhau, từ công nghiệp và y tế đến nông nghiệp và ngành điện tử. Dưới đây là bài viết về chủ đề: Cân bằng: Zn + HNO3 → Zn(NO3)2 + NO2 + H2O dễ hiểu, mời bạn đọc theo dõi.
Giáo dục
Giáo dục
Chủ đề liên quan
Bài viết
Phản ứng BaO + H2O tạo ra Ba(OH)2 thuộc loại phản ứng hóa hợp đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về BaO có lời giải, mời các bạn đón xem trong bài viết sau.
C6H5NH2 + HCl → C6H5NH3Cl đượcbiên soạn hướng dẫn các bạn viết phương Anilin tác dụng với HCl. Phương trình này cho thấy Anilin có tính bazo, tác dụng được với dung dịch axit và làm quỳ hóa đỏ.
CH2=CH-CH2-CH3 + HBr → CH3-CHBr-CH2-CH3 được biên soạn hướng dẫn bạn đọc viết và cân bằng chính xác phản ứng But-1-en tác dụng với dung dịch HBr dựa vào quy tắc Maccopnhicop để viết được sản phẩm chính. Mời các bạn tham khảo nội dung chi tiết phản ứng dưới đây.
FeCl3 + Ba(OH)2 → Fe(OH)3 + BaCl2 được biên soạn hướng dẫn bạn đọc viết và cân bằng chính xác phản ứng hóa học giữa muối và bazo. Cụ thể là khi cho FeCl3 tác dụng với dung dịch Ba(OH)2 sau phản ứng thu được kết tủa màu nâu đỏ của Fe(OH)3.
C2H3Cl → (-CH2CHCl-)n là phương trình điều chế nhựa PVC, hy vọng nội dung tài liệu sẽ giúp các bạn biết cách viết phương trình phản ứng C2H3Cl ra PVC cũng như vận dụng tốt vào các dạng câu hỏi bài tập liên quan.
FeCl2 + Cl2 → FeCl3 là phương trình phản ứng FeCl2 tạo ra FeCl3, khi cho FeCl2 tác dụng với Cl2. Xin mời bạn đọc tìm hiểu về phương trình này trong bài viết dưới đây.
FeS2 + H2SO4 → Fe2(SO4)3 + SO2 + H2O được biên soạn hướng dẫn bạn đọc viết và cân bằng phương trình phản ứng oxi hóa khử FeS2 tác dụng H2SO4 đặc nóng bẳng phương pháp thăng bằng electron. Chất khử sinh ra sau phản ứng thu được khí lưu huỳnh đioxit thoát ra.
Ba(OH)2 + H2SO4 → BaSO4 + H2O được biên soạn là phương trình phản ứng Ba(OH)2 tác dụng H2SO4 sau phản ứng thu được kết tủa trắng. Cũng như đưa ra các nội dung câu hỏi liên quan đến phản ứng Ba(OH)2+ H2SO4.
K + H2O → KOH + H2 được biên soạn hướng dẫn bạn đọc viết và cân bằng chính xác phản ứng Kali tác dụng H2O, sau phản ứng thu được dung dịch kiềm KOH, làm quỳ tím hóa xanh.
FeCl3 + KOH → Fe(OH)3 + KCl được biên soạn hướng dẫn các bạn học sinh viết và cân bằng phương trình phản ứng FeCl3 ra Fe(OH)3. Sau phản ứng thu được màu nâu đỏ. Mời các bạn tham khảo chi tiết nội dung tài liệu trong bài viết sau.
S + HNO3 → H2SO4 + NO2 + H2O được biên soạn là phương trình phản ứng oxi hóa khử, ở phương trình này lưu huỳnh đóng vai trò là chất khử. Mời các bạn xem chi tiết phản ứng tại bài viết sau đây.
H2S + NaOH → Na2S + H2O được biên soạn là phương trình hóa học cho H2S tác dụng NaOH sau phản ứng thu được muối Na2S. Hy vọng tài liệu giúp ích cho các bạn học sinh trong quá trình học tập và làm bài tập.
C2H5Cl + NaOH → C2H5OH + NaCl là phản ứng thế nguyên tử hidro halogenua bằng nhóm OH. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem trong bài viết dưới đây.
CO2 + H2O → H2CO3 biên soạn hướng dẫn các bạn học sinh viết và cân bằng phương trình phản ứng CO2 tác dụng với nước tạo ra dung dịch axit, làm quỳ tím chuyển sang màu đỏ. Hy vọng với nội dung tài liệu này sẽ giúp bạn đọc học tập tốt hơn, cũng như vận dụng tốt vào các dạng bài tập.
Phản ứng Cl2 + H2O ⇄ HCl + HClO là phản ứng oxi hóa khử. Clo trong phản ứng này không chỉ hoạt động như một chất oxi hóa mà còn đồng thời là một chất khử. Bài viết sau sẽ cung cấp đầy đủ thông tin về chi tiết đặc điểm phương trình hóa học này và các dạng bài tập liên quan, mời các bạn cùng tham khảo.
Phản ứng Cr + HCl hay Cr ra CrCl2 hoặc HCl ra CrCl2 thuộc loại phản ứng oxi hóa khử, phản ứng thế. Trong bài viết dưới đây còn có một số bài tập có liên quan về Phản ứng hóa học: Cr + HCl → CrCl2 + H2 ↑ | Cr ra CrCl2 có lời giải, mời các bạn đón xem.
Phản ứng hóa học: Fe + CuCl2 hay Fe ra FeCl2 hoặc Fe ra Cu hoặc CuCl2 ra Cu hoặc CuCl2 ra FeCl2 thuộc loại phản ứng oxi hóa khử và phản ứng thế. Xin mời bạn đọc theo dõi bài viết sau về Phản ứng hoá học Fe + CuCl2 → Cu + FeCl2.
Fe(OH)2 +O2 + H2O → Fe(OH)3 | Fe(OH)2 ra Fe(OH)3 là một phản ứng oxy hóa khử, được ứng dụng nhiều trong đời sống của con người. Xin mời bạn đọc cùng theo dõi bài viết sau về phản ứng hóa học Fe(OH)2 +O2 + H2O → Fe(OH)3.
Xem thêm