Metylamin (CH₃NH₂) là một hợp chất hữu cơ có công thức phân tử gồm một nguyên tử cacbon (C), ba nguyên tử hydro (H) và một nguyên tử nitơ (N). Nó còn được gọi là amin metyl hoặc amin metan. Dưới đây là bài viết về Tính chất hóa học, vật lý và ứng dụng của Metylamin CH5N, mời các bạn cùng tham khảo.
Mục lục bài viết
1. Tính chất hoá học của Metylamin:
– Tính Bazo: Dung dịch metylamin có khả năng làm xanh giấy quỳ tím hoặc làm hồng phenolphtalein do kết hợp với proton mạnh hơn amoniac. Amin có tính bazo yếu nên có thể phản ứng với các axit vô cơ để tạo thành muối
– Phản ứng với axit nitrơ: CH3-NH2 + HONO → CH3-OH + N2 + H2O (xúc tác HCl)
– Phản ứng ankyl hóa: CH3NH2 + CH3I → CH3NHCH3 + HI
– Phản ứng với dung dịch muối của các kim loại có hiđroxit kết tủa: 3CH3NH2 + FeCl3 + 3H2O → Fe(OH)3 + 3CH3NH3Cl
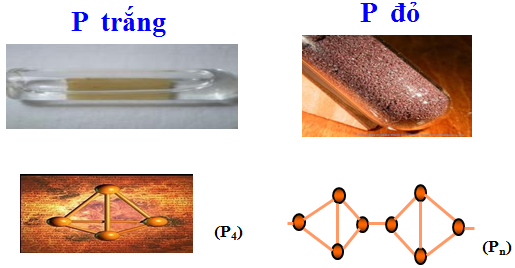
2. Tính chất vật lý của Metylamin:
– Metylamin là chất khí
– Có mùi khai khó chịu
– Là khí độc và tan tốt trong nước
3. Cách điều chế và ứng dụng của Metylamin trong đời sống:
Điều chế
– Thay thế nguyên tử H của phân tử amoniac
NH3 + CH3I → CH3-NH2 + HI
– Trong công nghiệp Metylamin được điều chế bằng phản ứng của amoniac với metanol
CH3OH + NH3 → CH3NH2 + H2O
Ứng dụng:
– Metylamin được coi là một bazơ yếu và được sử dụng rất phổ biến trong hóa học hữu cơ. Metylamin lỏng có đặc tính dung môi tương tự như amoniac lỏng.
– Các hóa chất có ý nghĩa được sản xuất từ meylamin bao gồm:
+ Dược phẩm: ephedrine và theophylline
+ Thuốc trừ sâu: carbofuran, carbaryl, và natri metam
+ Dung môi: N-methylformamide và N-methylpyrrolidone.
4. Bài tập liên quan kèm đáp án:
Ví dụ 1: Khi đốt cháy metylamin thu được H2O và CO2 với tỷ lệ số mol là
A. > 1. B. < 1.
C. = 1. D. không xác định được.
Hướng dẫn:
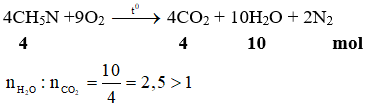
Đáp án: A
Ví dụ 2: Nhận định nào sau đây là sai?
A. Metylamin khi bị đốt cháy và tỏa nhiều nhiệt.
B. Đốt cháy metylamin, sau phản ứng thu được khí CO2 và hơi nước.
C. đốt cháy metylamin, số mol H2O thu được luôn lớn hơn số mol CO2.
D. Khi đốt cháy hoàn toàn metylamin, sản phẩm thu được làm đục nước vôi trong.
Hướng dẫn: Đốt cháy metylamin, sau phản ứng thu được khí CO2, N2 và hơi nước.
Đáp án: B
Ví dụ 3: Đốt cháy 1 mol khí metylamin trong không khí, sau phản ứng thu được khí CO2 và N2 có tổng số mol là
A. 1. B. 2.
C. 1,5. D. 2,5.
Hướng dẫn:
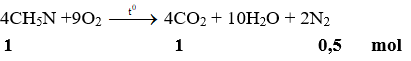
Đáp án: C
Ví dụ 4: Hòa tan hoàn toàn 1,93 gam hỗn hợp 2 kim loại Fe và Al vào dd HCl dư, sau phản ứng thu được m gam muối và 1,456 lít khí H2 ở đktc. Giá trị của m là:
A. 6,545 gam B. 5,46 gam C. 4,565 gam D. 2,456 gam
Giải:
Cách 1: nH2= 1,456/22,4= 0,065 mol
Các PTHH: 2Al + 6HCl→ 2AlCl3 + 3H2 (1)
Mol: x x 1,5x
Fe + 2HCl→ FeCl2 + H2 (2)
Mol: y y y
Theo đầu bài ta có: 27x + 56y = 1,93 (I) và 1,5x + y = 0,065 (II). Giải hệ (I) và (II) ta được:
x =0,03, y= 0,02 → m= 0,03.133,5 + 0,02. 127= 6,545 gam . Vậy đáp án A đúng
Cách 2: Ta luôn có nHCl=2nH2 = 2.0,065=0,13 mol. Vậy theo định luật bảo toàn khối lượng ta có:
1,93 + 0,13.36,5= m + 0,065.2 → m= 6,545 gam → Vậy đáp án A đúng
* Như vậy cách giải 2 ngắn gọn hơn và nhanh hơn rất nhiều cách 1, tuy nhiên muốn giải theo cách 2 chúng ta cần chú ý một số vấn đề sau:
– Trong các pư của kim loại, oxit… với axit thì : nHCl= 2nH2 hoặc nHCl = 2nH2O
Còn: nH2SO4= nH2=nH2O
nOH- = 2nH2 ( trong phản ứng của kim loại với H2O)
– Khi cho axit HCl tác dụng với muối cacbonat (CO32-) cần chú ý:
+ Khi cho từ từ HCl vào CO32- thì tứ tự phản ứng là:
CO32- + H+ → HCO3- sau đó khi HCl dư thì:
HCO3- + H+ → CO2 + H2O
+ Khi cho từ từ CO32- hoặc HCO3- vào dd HCl thì: xảy ra đồng thời cả 2 phản ứng
CO32- + 2H+ → H2O + CO2
HCO3- + H+ → CO2 + H2O
Ví dụ 5: Hoà tan hoàn toàn 2,81g hỗn hợp gồm Fe2O3, MgO, ZnO trong 500ml dd H2SO4 0,1M(vừa đủ).Sau phản ứng ,cô cạn dung dịch thu được muối khan có khối lượng là:
A. 6.81g
B. 4,81g
C.3,81g
D.5,81g
Ví dụ 6: Hoà tan hoàn toàn 3,22g hỗn hợp X gồm Fe, Mg Zn bằng một lượng vừa đủ H2SO4 loãng thấy thoát 1,344 lít H2 ở đktc và dung dịch chứa m gam muối. Giá trị của m là:
A. 10,27g
B.8.98
C.7,25g
D. 9,52g
Ví dụ 7: Hòa tan hết 6,3 gam hỗn hợp gồm Mg và Al trong vừa đủ 150 ml dung dịch gồm HCl 1M và H2SO4 1,5M thu được dung dịch X. Cô cạn dung dịch X thì thu được bao nhiêu gam muối khan?
A. 30,225 g
B. 33,225g
C. 35,25g
D. 37,25g
Ví dụ 8: Hoà tan 17,5 gam hợp kim Zn – Fe –Al vào dung dịch HCl thu được Vlít H2 đktc và dung dịch A Cô cạn A thu được 31,7 gam hỗn hợp muối khan . Giá trị V là ?
A. 1,12 lít
B. 3,36 lít
C. 4,48 lít
D. Kết quả khác
Ví dụ 9: Oxi hoá 13,6 gam hỗn hợp 2 kim loại thu được m gam hỗn hợp 2 oxit . Để hoà tan hoàn toàn m gam oxit này cần 500 ml dd H2SO4 1 M . Tính m .
A. 18,4 g
B. 21,6 g
C. 23,45 g D. Kết quả khác
Ví dụ 10: Hoà tan 10g hỗn hợp bột Fe và Fe2O3 bằng một lượng dd HCl vừa đủ, thu được 1,12 lít hiđro (đktc) và dd A cho NaOH dư vào thu được kết tủa, nung kết tủa trong không khí đến khối lượng không đổi được m gam chất rắn thì giá trị của m là:
A. 12g
B. 11,2g
C. 12,2g
D. 16g
Ví dụ 11: Đốt cháy hết 2,86 gam hỗn hợp kim loại gồm Al, Fe, Cu được 4,14 gam hỗn hợp 3 oxit . Để hoà tan hết hỗn hợp oxit này, phải dùng đúng 0,4 lít dung dịch HCl và thu được dung dịch X. Cô cạn dung dich X thì khối lượng muối khan là bao nhêu ? .
A. 9,45 gam
B.7,49 gam
C. 8,54 gam
D. 6,45 gam
Ví dụ 12: Cho 24,12gam hỗn hợp X gồm CuO , Fe2O3 , Al2O3 tác dụng vừa đủ với 350ml dd HNO3 4M rồi đun đến khan dung dịch sau phản ứng thì thu được m gam hỗn hợp muối khan. Tính m .
A. 77,92 gam
B.86,8 gam
C. 76,34 gam
D. 99,72 gam
Ví dụ 13: Hòa tan 9,14 gam hợp kim Cu, Mg, Al bằng một lượng vừa đủ dung dịch HCl thu được 7,84 lít khí X (đktc) và 2,54 gam chất rắn Y và dung dịch Z. Lọc bỏ chất rắn Y, cô cạn cẩn thận dung dịch Z thu được lượng muối khan là
A. 31,45 gam.
B. 33,99 gam
C. 19,025 gam
D. 56,3 gam
Ví dụ 14: Cho 40 gam hỗn hợp vàng, bạc, đồng, sắt, kẽm tác dụng với O2 dư nung nóng thu được 46,4 gam hỗn hợp X. Cho hỗn hợp X này tác dụng vừa đủ dung dịch HCl cần V lít dung dịch HCl 2M.Tính V.
A. 400 ml
B. 200ml
C. 800 ml
D. Giá trị khác.
Ví dụ 15: Hòa tan m gam hỗn hợp gồm Cu và Fe3O4 trong dung dịch HCl dư sau phản ứng còn lại 8,32 gam chất rắn không tan và dung dịch X. Cô cạn dung dịch X thu được 61,92 gam chất rắn khan. Giá trị của m
A. 31,04 gam
B. 40,10 gam
C. 43,84 gam
D. 46,16 gam
Ví dụ 16: Cho m gam hỗn hợp Cu và Fe2O3 trong dung dịch H2SO4 loãng dư thu được dung dịch X và
0,328 m gam chất rắn không tan. Dung dịch X làm mất màu vừa hết 48ml dung dịch KMnO4 1M. Giá trị của m là
A. 40 gam
B. 43,2 gam
C. 56 gam
D. 48 gam
Ví dụ 17: Hòa tan hoàn toàn 14,6 gam hỗn hợp X gồm Al và Sn bằng dung dịch HCl (dư), thu được 5,6 lít H2(ở đktc). Thể tích khí O2 (ở đktc) cần để phản ứng hoàn toàn với 14,6 gam hỗn hợp X là
A. 3,92 lít.
B. 1,68 lít
C. 2,80 lít
D. 4,48 lít
Ví dụ 18: Hỗn hợp X gồm 2 kim loại A và B thuộc phân nhóm chính nhóm II, ở 2 chu kỳ liên tiếp. Cho 1,76 gam X tan hoàn toàn trong dung dịch HCl dư thu được 1,344 lít khí H2 (đktc). Cô cạn dung dịch sau phản ứng, khối lượng muối khan thu được là
A. 6,02 gam.
B. 3,98 gam.
C. 5,68 gam.
D. 5,99 gam.
Ví dụ 19: Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10% thu được 2,24 lít khí H2 (ở đktc). Khối lượng dung dịch thu được sau phản ứng là
A. 101,68 gam.
B. 88,20 gam.
C. 101,48 gam.
D. 97,80 gam.
Ví dụ 20: Cho hỗn hợp gồm Fe và FeS tác dụng với dung dịch HCl dư thu được 2,24 lít hỗn hợp khí ở điều kiện tiêu chuẩn. Hỗn hợp khí này có tỉ khối so với hiđro là 9. Thành phần % theo số mol của hỗn hợp Fe và FeS ban đầu lần lượt là
A. 40% và 60%.
B. 50% và 50%.
C. 35% và 65%.
D. 45% và 55%.
Ví dụ 21: Cho 3,87 gam Mg và Al vào 200ml dung dịch X gồm HCl 1M và H2SO4 0,5M thu được dung dịch B và 4,368 lít H2 ở đktc. Phần trăm khối lượng của Mg và Al trong hỗn hợp lần lượt là
A. 72,09% và 27,91%.
B. 62,79% và 37,21%.
C. 27,91% và 72,09%.
D. 37,21% và 62,79%.
Ví dụ 22: Cho 40 gam hỗn hợp vàng, bạc, đồng, sắt, kẽm tác dụng với O2 dư nung nóng thu được m gam hỗn hợp X. Cho hỗn hợp X này tác dụng vừa đủ dung dịch HCl cần 400 ml dung dịch HCl 2M (không có H2 bay ra). Tính khối lượng m.
A. 46,4 gam
B. 44,6 gam
C. 52,8 gam
D. 58,2 gam
Ví dụ 23: Cho 20 gam hỗn hợp một số muối cacbonat tác dụng hết với dung dịch HCl dư thu được 1,344 lít khí CO2 (đktc) và dung dịch A. Cô cạn dung dịch A thu được m gam muối khan. Giá trị của m là
A. 10,33 gam
B. 20,66 gam
C. 25,32 gam
D. 30 gam
Ví dụ 24: Cho 23,8 gam hỗn hợp hai muối cacbonat của hai kim loại A, B tác dụng hết với dung dịch HCl dư thu được V lít khí CO2 (đktc) và dung dịch A. Dẫn toàn bộ CO2 vào dd nước vôi trong dư thì thu được 20 gam kết tủa. Cô cạn dung dịch A thu được m gam muối khan. Giá trị của m là
A. 26 gam
B. 30 gam
C. 23 gam
D. 27 gam
Ví dụ 25: Cho m gam hỗn hợp hai muối cacbonat của hai kim loại A, B tác dụng hết với dung dịch HCl dư thu được 4,48 lít khí CO2 (đktc) và dung dịch A. Cô cạn dung dịch A thu được 26 gam muối khan. Giá trị của m là
A. 23,8 gam
B. 25,2 gam
C. 23,8 gam
D. 27,4 gam
Ví dụ 26: Hoà tan hoàn toàn 3,34 gam hỗn hợp hai muối cacbonat trung hòa của hai kim loại hóa trị II và III bằng dung dịch HCl dư thì thu được dung dịch A và 0,896 lít bay ra (đktc). Khối lượng muối có trong dung dịch A là
A. 31,8 gam
B. 3,78 gam
C. 4,15 gam
D. 4,23 gam
Ví dụ 27: Cho 11,5g hỗn hợp gồm ACO3, B2CO3, R2CO3 tan hết trong dung dịch HCl thu được 2,24 lít CO2(đktc). Khối lượng muối clorua tạo thành là?
A. 16,2g
B. 12,6g
C. 13,2g
D. 12,3g
Ví dụ 28: Hòa tan hoàn toàn 10 gam hỗn hợp hai muối XCO3 và Y2(CO3)3 bằng dung dịch HCl ta thu được dung dịch A và 0,672 lít khí bay ra ở đktc. Cô cạn dung dịch A thì thu được m gam muối khan. Giá trị của m là
A. 1,033 gam.
B. 10,33 gam.
C. 9,265 gam.
D. 92,65 gam.
Ví dụ 29: Hoà tan hoàn toàn 19,2 hỗn hợp gồm CaCO3 và MgCO3 trong dung dịch HCl dư thấy thoát ra V (lít) CO2 (đktc) và dung dịch có chứa 21,4 gam hỗn hợp muối. Xác định V.
A. V = 3,36 lít
B. V = 3,92 lít
C. V = 4,48 lít
D.V = 5,6 lít
Ví dụ 30: Hòa tan hết hỗn hợp hai kim loại kiềm thổ vào nước, có 1,344 lít H2 (đktc) thoát ra và thu được dung dịch X. Thể tích dung dịch HCl 1M cần để trung hòa vừa đủ dung dịch X là:
A .12 ml
B. 120 ml
C. 240 ml
D. Tất cả đều sai
Ví dụ 31: Hòa tan 2 kim loại Ba và Na vào nước được dd(A) và có 13,44 lít H2 bay ra (đktc). Thể tích dung dịch HCl 1M cần để trung hòa hoàn toàn dd A là:
A.1,2lít
B.2,4lít
C.4,8lít
D.0,5lít.
Ví dụ 32: Khối lượng hỗn hợp A gồm K2O và BaO (tỉ lệ số mol 2 : 3) cần dùng để trung hòa hết 1,5 lít dung dịch hỗn hợp B gồm HCl 0,005M và H 2SO4 0,0025M là
A. 0,0489 gam.
B. 0,9705 gam.
C. 0,7783 gam.
D. 0,1604 gam.
Ví dụ 33: Cho từ từ 100 ml dung dịch HCl 0,5 M vào 150 ml dung dịch Na2CO3 0,2 M thu được V lít khí CO2 ( đktc). Giá trị của V là:
A. 0,448
B. 0,336
C. 0,224
D. 0,56
Ví dụ 34: Cho từ từ 200 ml dung dịch HCl 0,2 M vào 100 ml dd X chứa Na2CO3 0,2 M và NaHCO3 0,1 M thu được V lít khí CO2 ở đktc. Giá trị của V là:
A. 0,672
B. 0,336
C. 0,224
D. 0,448
THAM KHẢO THÊM: