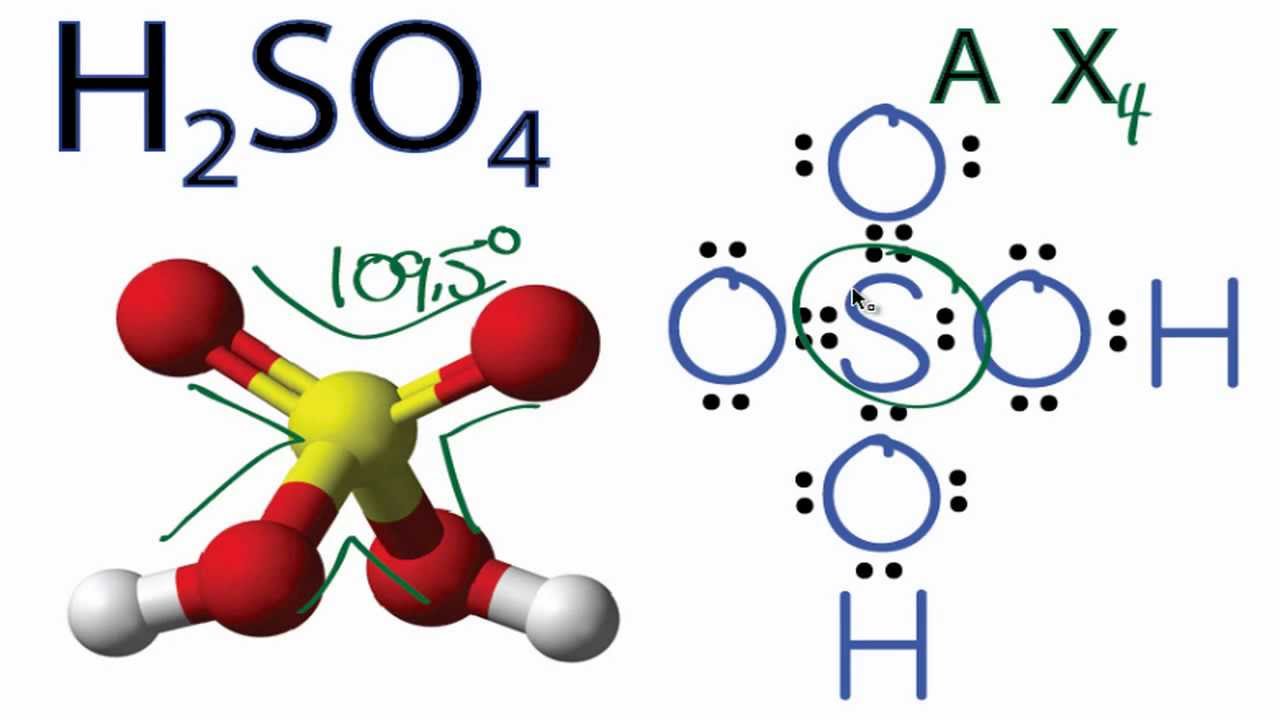
Ag + H2SO4 → Ag2SO4 + SO2 + H2O là phản ứng được gọi là phản ứng oxi hóa khử, trong đó Ag và H2SO4 là chất khử và oxi hóa, tương ứng. Khi thực hiện phản ứng này, các chất khử và oxi hóa sẽ tương tác với nhau để tạo ra các sản phẩm mới như Ag2SO4, SO2 và H2O.