Phản ứng Ba(OH)2 + NH4Cl tạo ra Ba(OH)2 và khí NH3 bay lên thuộc loại phản ứng trao đổi đã được cân bằng chính xác và chi tiết nhất. Bên cạnh đó là một số bài tập có liên quan về Ba(OH)2 có lời giải, mời các bạn đón xem:
Mục lục bài viết
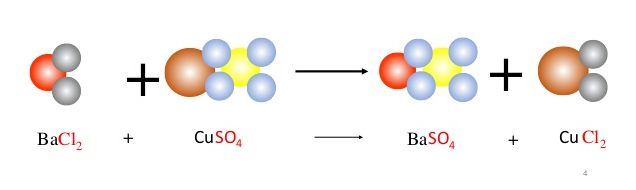
1. Phản ứng hoá học Ba(OH)2 + NH4Cl → BaCl2 + NH3 + H2O:
Phương trình Ba(OH)2 + NH4Cl -> NH3 + H2O sau khi tiến hành cân bằng phương trình hóa học thì ta được phương trình như sau:
Ba(OH)2 + 2NH4Cl -> BaCl2 + 2NH3 + 2H2O
Điều kiện phản ứng:
– Không có
Cách thực hiện phản ứng:
– Cho dung dịch Ba(OH)2 tác dụng với NH4Cl
Hiện tượng nhận biết phản ứng:
– Khi cho bari hiđroxit phản ứng với amoni clorua sinh ra khí có mùi khai amoniac
Bạn có biết:
Tương tự Ba(OH)2, các bazơ khác như NaOH, KOH, Ca(OH)2 cũng có phản ứng với NH4Cl tạo khí NH3
Khi cho bari hidroxit phản ứng với amoni clorua sinh ra khí có mùi khai amoniac. Theo đó thì Khí amoniac có mùi khai và gây kích thích đối với mũi, vì vậy khi phản ứng xảy ra, mùi khai amoniac sẽ được cảm nhận.
Các bazơ như NaOH (natri hidroxit), KOH (kali hidroxit), Ca(OH)2 (canxi hidroxit), và các bazơ khác cũng thường có khả năng phản ứng với amoni clorua (NH4Cl) để tạo ra khí amoniac (NH3) và nước (H2O). Cụ thể, các phản ứng này có thể được biểu diễn như sau:
NaOH + NH4Cl→NaCl + NH3 + H2O
KOH + NH4Cl→ KCl + NH3 + H2O
Ca(OH)2 + 2NH4Cl → CaCl2 + 2NH3 + 2H2O
Trong các phản ứng trên, bazơ tác dụng với amoni clorua để tạo ra muối và khí amoniac. Khí amoniac sinh ra có mùi khai và thường được nhận diện dễ dàng.
2. Tính chất hóa học của Ba(OH)2:
Tính chất hóa học của các chất tham gia phản ứng trong phương trình Ba(OH)2 + NH4Cl -> BaCl2 + NH3 + H2O. Căn cứ dựa theo phương trình trên thì ta thấy rằng chất tham gia ở đây chính là Ba(OH)2 và NH4Cl
Đầu tiên đó là về tính chất hóa học của Ba(OH)2 . Tính chất nổi bật nhất khi nhắc đến Ba(OH)2 đó là mang đầy đủ tính chất của một bazo mạnh
Phản ứng với axit: Ba(OH)2 + 2HCl→BaCl2 +2H2O
Phản ứng với oxit axit (SO₂, CO₂):
Ba(OH)2 + SO2 →BaSO3 + H2O
Phản ứng với axit hữu cơ tạo thành muối: 2CH3COOH + Ba(OH)2 → (CH3COO)2Ba + 2H2O
Phản ứng thủy phân este: 2CH3COOC2H5 + Ba(OH)2 → (CH3COO)2Ba + 2C2H 5OH
Phản ứng với muối: Ba(OH)2 +CuCl2 →BaCl2 +Cu(OH)2 ↓
Tác dụng với một số kim loại mà oxit, hidroxit của chúng có tính lưỡng tính (Al, Zn…):
Ba(OH) 2 + 2Al + 2H2O→Ba(AlO2)2 +3H2 ↑
Tác dụng với hợp chất lưỡng tính:
Ba(OH)2 + 2Al(OH)3 → Ba(AlO2)2 +4H2O
Ba(OH)2 +Al2O3 → Ba(AlO2)2 +H2
Các phản ứng này thường phản ánh tính chất của bari hidroxit là một bazơ mạnh và có khả năng tương tác với nhiều loại hợp chất khác nhau.
3. Tính chất hóa học của NH4Cl:
Phân hủy khi đun nóng: NH4Cl→ NH3 + HCl Amoni clorua có khả năng thăng hoa khi bị đun nóng, thực chất, phản ứng này dẫn đến phân hủy thành amoniac (NH₃) và axit hydrocloric (HCl).
Phản ứng với bazơ mạnh (NaOH) để giải phóng khí amoniac: NH4Cl + NaOH→NH3 +NaCl+H2O Amoni clorua phản ứng với bazơ mạnh như hidroxit natri (NaOH) để tạo ra khí amoniac (NH₃), muối (NaCl), và nước (H₂O).
Tác dụng với cacbonat kim loại kiềm ở nhiệt độ cao: NH4Cl + NaCO3 → 2NaCl + CO2 +H2O+2NH3 Amoni clorua có thể phản ứng với các carbonate kim loại kiềm ở nhiệt độ cao, tạo ra khí amoniac (NH₃), muối (NaCl), khí CO2 và nước.
Độ pH của dung dịch 5% amoni clorua: Dung dịch amoni clorua 5% trong nước có độ pH khoảng từ 4.6 – 6.0 và làm quỳ tím chuyển sang màu đỏ, chỉ ra tính axit của dung dịch. Những tính chất này là quan trọng trong việc hiểu về tính chất hóa học của amoni clorua và cách nó tương tác với các chất khác trong các điều kiện khác nhau.
4. Bài tập vận dụng kèm lời giải:
Câu 1: Hãy cho chúng tôi biết dung dịch chất nào sau đây tác dụng với dung dịch Ba(OH)2 tạo ra kết tủa
A. NaCl
B. Ca(HCO3)2
C. KCl
D. KNO3
Hướng dẫn giải:
Chính xác, đáp án là B.
Phản ứng xảy ra giữa dung dịch Ba(OH)₂ và dung dịch Ca(HCO₃)₂ tạo ra kết tủa các muối cacbonat:
Ca(HCO3)2 + Ba(OH)2 → CaCO3 + BaCO3 + 2H2O
Kết tủa được tạo thành bao gồm canxi cacbonat (CaCO₃) và bari cacbonat (BaCO₃). Cả hai muối này là chất ít hòa tan và sẽ kết tụ thành kết tủa trong dung dịch.
Câu số 2: Hãy chọn đáp án đúng nhất trong những phương án sau:
Bari có cấu trúc tinh thể theo kiểu nào?
A. Lập phương tâm khối
B. Lục phương
C. Lập phương tâm diện
D. Khác
Hướng dẫn giải:
Đáp án là A. Bari thường có cấu trúc tinh thể theo kiểu lập phương tâm khối. Cấu trúc này thường được mô tả như một lưới lập phương với các nguyên tử hoặc ion bari tại các tâm của các khối lập phương.
Câu số 3: Biết rằng khi nhiệt phân muối NH4NO3 thì ta sẽ thu được khí A và H2O vậy khí A trong trường hợp này là gì?
A. N2
B. N2O
C. NO2
D. N2O5
Hướng dẫn giải:
đáp án là B. Khi nhiệt phân muối NH₄NO₃, ta thu được khí N2O (nitrous oxide) và nước ( H2O).
NH4NO3 → N2O + 2H2O
Vậy nếu muốn biết khí A là gì, thì đó chính là khí nitrous oxide ( N2O).
Câu hỏi số 4: Hãy trả lời nội dung câu hỏi sau: Khi tiến hành nung chất rắn A ở nhiệt độ cao thì người ta thu được một oxit của nito và hơi nước, và cho A vào dung dịch KOH thì ta thấy có mùi khai thoát ra. Vậy bạn hãy cho chúng tôi biết A là gì?
A. (NH4)2SO4.
B. NH4NO2.
C. NH4HCO3.
D. NH4NO3.
Hướng dẫn giải:
Đáp án là D. Khi nung chất rắn NH4NO3 (amoni nitrat) ở nhiệt độ cao, ta thu được oxit của nitơ và hơi nước: NH4NO3 → N2O + 2H2O
Sau đó, khi chất NH4NO3 được đưa vào dung dịch KOH, khí mùi khai thoát ra, và đó chính là khí amoniac ( NH3 ): NH4NO3 + KOH → N2O + 2H2O + NH3
Do đó, NH4NO3 là chất A trong trường hợp này
Câu 5: Theo đó thì dung dịch tác dụng được với Fe(NO3)2 và CuCl2
A. dung dịch NaOH
B. dung dịch HCl
C. dung dịch AgNO3
D. dung dịch BaCl2
Hướng dẫn giải:
đáp án là A.
Dung dịch tác dụng được với các dung dịch 2Fe(NO3)2 và CuCl2 là dung dịch NaOH:
Fe(NO3)2 + 2NaOH → Fe(OH)2↓+ 2NaNO3
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
Cả hai phản ứng đều tạo ra kết tủa hydroxide của kim loại.
Câu 5: Tiến hành cho dung dịch NaOH vào ống nghiệm đựng dung dịch FeCl3 hiện tượng quan sát được đó là
A. Dung dịch trong suốt
B. Xuất hiện kết tủa màu nâu đỏ
C. Sẽ xuất hiện kết tủa màu trắng xanh
D. Xuất hiện kết tủa trắng
Hướng dẫn giải;
Đáp án là B. Khi dung dịch NaOH được thêm vào dung dịch FeCl3, phản ứng sẽ tạo ra kết tủa hydroxide sắt thủy nâu đỏ: FeCl3 + 3NaOH→Fe(OH)3↓ + 3NaCl
Kết tủa này có màu nâu đỏ và là biểu hiện của sự tạo thành hydroxide sắt.
Câu số 6: Bạn hãy cho chúng tôi biết về ứng dụng của NH4Cl ?
Hướng dẫn trả lời:
Phân bón: Amoni chloride được sử dụng chủ yếu như một nguồn cung cấp nitơ trong phân bón, đặc biệt là trong sản xuất amoni clorophotphat. Loại phân bón này thường được sử dụng cho cây trồng như lúa ở châu Á.
Pháo hoa: Amoni chloride đã từng được sử dụng trong pháo hoa vào thế kỷ 18 để cung cấp nguồn clo, giúp tăng cường màu xanh lá cây và màu xanh da trời từ ion đồng trong ngọn lửa.
Khói trắng trong quân sự: Trong quá khứ, amoni chloride được sử dụng để tạo ra khói trắng. Tuy nhiên, do phản ứng phân hủy nhanh chóng với kali clorat, tạo ra hợp chất amoni clorat không ổn định, nên việc sử dụng chất này trong mục đích này đã bị hạn chế. Amoni chloride đã được sử dụng trong quá khứ để tạo ra khói trắng cho các mục đích quân sự và phương tiện giao thông, tạo ra màn khói màu trắng để che phủ hoạt động quân sự và địa điểm chiến trận. Tuy nhiên, việc sử dụng amoni chloride trong mục đích này đã bị hạn chế do khả năng phân hủy nhanh chóng khi tiếp xúc với kali clorat. Phản ứng giữa amoni chloride và kali clorat tạo ra hợp chất amoni clorat, nhưng hợp chất này không ổn định và có thể dẫn đến hiện tượng nổ. Do đó, để đảm bảo an toàn, các chất thay thế an toàn hơn đã được phát triển để thay thế amoni chloride trong ứng dụng tạo khói trắng trong quân sự.
Các ứng dụng này thể hiện tính chất đa dạng của amoni chloride trong các lĩnh vực khác nhau như nông nghiệp và công nghiệp hóa chất.