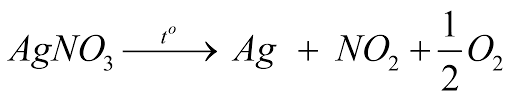Khi nhiệt phân hoàn toàn NaNO3, phản ứng sẽ tạo ra một chất rắn mới. Chất rắn này có công thức hóa học là NaNO2. Vì vậy, khi thực hiện phản ứng nhiệt phân hoàn toàn NaNO3, chúng ta sẽ thu được chất rắn NaNO2. Điều này có nghĩa là toàn bộ NaNO3 đã phân hủy và chuyển hóa thành chất rắn mới có công thức NaNO2.
Mục lục bài viết
1. Nhiệt phân hoàn toàn NaNO3 thì chất rắn thu được:
Nhiệt phân hoàn toàn NaNO3 thì chất rắn thu được là?
A. NaNO2
B. NaOH
C. Na2O
D. Na
Đáp án A
NaNO3 → NaNO2 + ½ O2
Khi nhiệt phân hoàn toàn NaNO3, một phản ứng hóa học xảy ra để tạo ra các sản phẩm mới. Trong quá trình này, chất rắn NaNO3 sẽ phân hủy và tạo ra muối NaNO2 cùng với việc giải phóng một loại khí không màu gọi là O2. Điều này có nghĩa là chất rắn NaNO3 đã chuyển hóa thành hai chất mới, bao gồm muối NaNO2 và khí O2. Quá trình nhiệt phân hoàn toàn này có thể xem như một phương pháp chuyển đổi chất rắn thành các thành phần khác nhau, và đồng thời tạo ra một loại khí mới có tính chất không màu. Nên chọn đáp án A.
2. Điều kiện phản ứng nhiệt phân NaNO3 xảy ra:
Nhiệt độ là yếu tố quan trọng trong quá trình phản ứng nhiệt phân của NaNO3. Khi nhiệt độ tăng lên, tốc độ phản ứng cũng tăng lên do năng lượng cung cấp cho phản ứng nhiệt phân tăng. Điều này có nghĩa là nếu nhiệt độ không đủ cao, phản ứng nhiệt phân NaNO3 không thể xảy ra hoặc xảy ra rất chậm. Tuy nhiên, nếu nhiệt độ quá cao, có thể gây hiện tượng phá hủy các chất tham gia phản ứng. Do đó, cần điều chỉnh nhiệt độ phù hợp để đảm bảo phản ứng nhiệt phân NaNO3 xảy ra một cách hiệu quả và an toàn trong thí nghiệm.
3. Nhiệt phân muối nitrat (NO3-):
Muối nitrat có tính kém bền nhiệt, do đó khi nung nóng, muối nitrat sẽ bị nhiệt phân và tạo ra các sản phẩm khác. Quá trình tạo ra sản phẩm này phụ thuộc vào kim loại tạo thành muối nitrat.
Nhiệt phân muối nitrat xảy ra thông qua một quá trình hóa học gọi là phân hủy nhiệt. Trong quá trình này, muối nitrat tham gia phản ứng phân hủy và tạo ra các chất khí, chất lỏng hoặc chất rắn mới. Các chất sản phẩm có thể là oxit kim loại, nitơ, oxi hoặc các hợp chất khác.
Muối nitrat có thể được tạo thành từ nhiều kim loại khác nhau như kali nitrat (KNO3), natri nitrat (NaNO3) hoặc amonium nitrat (NH4NO3). Mỗi loại muối nitrat sẽ có quá trình nhiệt phân riêng biệt và tạo ra các sản phẩm khác nhau.
Việc hiểu quá trình nhiệt phân muối nitrat rất quan trọng trong nhiều ngành công nghiệp và ứng dụng khác nhau. Nó có thể được áp dụng trong việc sản xuất phân bón, thuốc nổ, pháo hoa và cả trong quá trình sản xuất thép và thủy tinh.
Vì vậy, để nghiên cứu và ứng dụng hiệu quả nhiệt phân muối nitrat, chúng ta cần hiểu rõ cơ chế và quá trình phản ứng của nó với các kim loại khác nhau. Điều này sẽ giúp chúng ta tận dụng tối đa tiềm năng của muối nitrat và tạo ra các sản phẩm có giá trị cao hơn.
Nhiệt phân muối nitrat của kim loại trung bình (từ Mg đến Cu)
Muối nitrat → Oxit kim loại + NO2 + O2
2M(NO3)n → M2On + 2nNO2 + n/2O2
Ví dụ: 2Cu(NO3)2 → 2CuO + 4NO2 + O2
Nhiệt phân muối nitrat của kim loại đứng trước Mg (Li, K, Ba, Ca, Na)
Muối nitrat → Muối nitrit và O2
2M(NO3)n → 2M(NO2)n + nO2
Ví dụ: 2NaNO3 → 2NaNO2 + O2
Nhiệt phân muối nitrat của kim loại sau Cu
Muối nitrat → kim loại + NO2 + O2
M(NO3)n → M + nNO2 + n/2O2
Ví dụ: 2AgNO3 → 2Ag + 2NO2 + O2
Một số phản ứng đặc biệt
2Fe(NO3)3 → Fe2O3 + 6NO2 + 3/2O2
NH4NO3 → N2O + 2H2O
NH4NO2 → N2 + 2H2O
4. Bài tập vận dụng liên quan:
Câu 1. Nhiệt phân hoàn toàn NaNO3 thì chất rắn thu được là
A. NaNO2
B. NaOH
C. Na2O
D. Na
Hướng dẫn giải
Đáp án A
Khi nhiệt phân hoàn toàn NaNO3, quá trình này sẽ tạo ra chất rắn NaNO2. Trong quá trình này, NaNO3 được chuyển đổi thành NaNO2 thông qua phản ứng nhiệt phân. Quá trình nhiệt phân NaNO3 là quá trình giải phân tử NaNO3 thành các phân tử NaNO2. Do đó, kết quả của quá trình nhiệt phân hoàn toàn NaNO3 là có chất rắn NaNO2 được hình thành.
2NaNO3 → 2NaNO2 + O2↑
Câu 2. Khi nhiệt phân muối NaNO3 thu được các chất là:
A. NaNO2, N2 và O2
B. NaNO2 và O2
C. NaNO2 và NO2
D. NaNO2, N2 và CO2
Hướng dẫn giải
Đáp án B
Quá trình nhiệt phân muối NaNO3 là một phản ứng hóa học quan trọng, trong đó muối NaNO3 được phân hủy thành hai chất riêng biệt là NaNO2 và O2. Khi áp dụng nhiệt, các liên kết trong muối NaNO3 bị phá vỡ, tạo ra cation Na+ và anion NO3-. Cation Na+ tương tác với nước trong môi trường, tạo thành ion Na+ và OH-. Trong khi đó, anion NO3- bị phân tách thành hai chất là NO2 và O2.
Chất NO2 là một chất khí nâu đỏ có mùi hắc và độc. Đây là một chất dễ cháy và có thể tạo thành các tác nhân ôxi hóa mạnh. Chất O2 là một khí không màu, không mùi, và có khả năng hỗ trợ cháy. Đây là một chất quan trọng trong quá trình hô hấp của sinh vật và trong nhiều ứng dụng công nghiệp.
2NaNO3 → 2NaNO2 + O2↑
Câu 3. Đem nung một m gam Cu(NO3)2 sau một thời gian dừng lại, làm nguội, rồi cân thấy khối lượng giảm 5,4 gam. Vậy khối lượng muối Cu(NO3)2 đã bị nhiệt phân là:
A. 9,4 gam
B. 0,94 gam
C. 4,7 gam
D. 0,47 gam
Hướng dẫn giải
Đáp án A
Phương trình phản ứng nhiệt phân
2Cu(NO3)2 → 2CuO + 4NO2 + O2
x → x → 2x → 0,5x
mgiảm= mkhí sinh ra= mNO2+ mO2 => 2x.46 + 0,5x.32 = 5,4 => x = 0,05 mol
=> mCu(NO3)2 = 0,05. (64 + 14.2 + 16.3.2) = 9,4 gam
Câu 4. Nhiệt phân hoàn toàn 9,4 gam muối nitrat của kim loại R thu được 4 gam chất rắn. Công thức của muối là.
A. Pb(NO3)2.
B. Fe(NO3)2.
C. Cu(NO3)2.
D. AgNO3.
Hướng dẫn giải
Đáp án D
Ở dạng bài tập này, bạn đọc phải chia thành 3 trường hợp xảy ra, bởi vì đối với muối nitrat của các nhóm kim loại khác nhau, khi nhiệt phân xảy ra, sẽ tạo ra các chất khác nhau. Ví dụ, muối nitrat của kim loại A có thể tạo ra chất X trong khi muối nitrat của kim loại B có thể tạo ra chất Y. Điều này cho thấy sự đa dạng và sự phụ thuộc vào nhóm kim loại mà muối nitrat thuộc về. Do đó, việc phân tích và hiểu rõ các trường hợp khác nhau này là rất quan trọng để hiểu quy luật và tính chất của các chất muối nitrat.
Ta xét lần lượt các trường hợp dưới đây
Trường hợp 1: sản phẩm nhiệt phân là muối nitrit và oxi.
mO2 = 9,4 −4 = 5,4 gam
⇒ nO2 = 5,4/32 = 0,16875 (mol)
Phương trình phản ứng nhiệt phân
M(NO3)n → M(NO2)n+ 1/2nO2
⇒ nM(NO3)n = 0.,3375n (mol)
MM(NO3)n = 9,4n/0,3375 =27,8n (loại)
Trường hợp 2: sản phẩm nhiệt phân là oxit, NO2 và O2
Phương trình phản ứng nhiệt phân
2M(NO3)n → M2On + 2nNO2 + 1/2nO2
nM(NO3)n= 9,4/(M + 62n)
⇒ nM2On = 4,7/(M + 62n)
⇒ 4,7/(M + 62n) = 4/(2M + 16n)
⇔ 4 (M + 62n) = 4,7(2M + 16n)
⇔ M = 32n
n = 2 ⇒ M = 64 (Cu)
Công thức thỏa mãn là Cu(NO3)2
Trường hợp 3: sản phẩm nhiệt phân là kim loại, NO2 và O2
Phương trình phản ứng nhiệt phân
M(NO3)n → M + nNO2 + 1/2nO2
nM(NO3)n = nM
⇒ 9,4/(M + 62n)= 4/M
⇔ 9,4/M = 4/(M + 62n)
⇔M = 45,93 n (loại)
Câu 5. Nung nóng 66,2 gam Pb(NO3)2 thu được 55,4 gam chất rắn. Tính hiệu suất của phản ứng phân hủy.
A. 50%
B. 70%
C. 55%
D. 75%
Hướng dẫn giải
Đáp án A
Phương trình phản ứng
Pb(NO3)2 → PbO + 2NO2 + 1/2O2
mNO2 + mO2 = 46.2x + 32.0,5x = 66,2 – 55,4 => x = 0,1 mol
Khối lượng của Pb(NO3)2 phản ứng là:
mPb(NO3)2 = 0,1.331 = 33,1 gam
Hiệu suất phản ứng thủy phân là: H = 33,1/66,2.100% = 50%
Câu 6. Khi bị nhiệt phân, dãy muối nitrat nào sau đây đều cho sản phẩm là kim loại, khí nitơ đioxit và khí oxi?
A. Zn(NO3)2, NaNO3, Fe(NO3)2
B. Ca(NO3)2, NaNO3, KNO3
C. Cu(NO3)2, LiNO3, KNO3
D. Hg(NO3)2, AgNO3
Hướng dẫn giải
Đáp án D
Dãy muối nitrat đều cho ra sản phẩm là kim loại, khí nitơ đioxit và khí oxi. Ví dụ như Hg(NO3)2 và AgNO3. Muối nitrat là một loại hợp chất hóa học được tạo thành từ nitrat và một kim loại. Chúng thường được sử dụng trong các ứng dụng công nghiệp, nông nghiệp và y tế. Muối nitrat cũng có thể được sử dụng trong sản xuất thuốc nổ và pháo hoa. Kim loại và khí tạo thành từ dãy muối nitrat đóng vai trò quan trọng trong các quá trình hóa học và ngành công nghiệp khác nhau.
2AgNO3 → 2Ag + 2NO2 + O2
2Hg(NO3)2 → 2HgO + 4NO2 + O2
Câu 7. Cho lượng khí NH3 đi từ từ qua ống sứ chứa 3,2 gam CuO nung nóng đến khi phản ứng xảy ra hoàn toàn ; thu được rắn X và 1 hỗn hợp khí Y. Chất rắn A phản ứng vừa đủ với 20 ml HCl 1M. Tính thể tích khí N2 (đktc) tạo thành sau phản ứng là
A. 1,12 lít
B. 2,24 lít
C. 4,48 lít
D. 6,72 lít
Hướng dẫn giải
Đáp án B
2NH3 + 3CuO → 3Cu + N2↑ + 3H2O
Chất rắn A: Cu và CuO dư
CuO + 2HCl → CuCl2 + H2O
nCuO = nHCl/2 = 0,02/2 = 0,01 mol
số mol CuO tham gia phản ứng khử là: 3,2/80 – 0,01= 0,03 mol
⇒ VN2= 0,01. 22,4 = 2,24 lít
Câu 8. Nhiệt phân hoàn toàn Fe(NO3)2 trong không khí thu được sản phẩm gồm
A. FeO, NO2, O2.
B. Fe2O3, NO2.
C. Fe2O3, NO2, O2.
D. Fe, NO2, O2.
Hướng dẫn giải
Đáp án C
Vì Fe là kim loại trung bình nên sản phẩm thu được gồm oxit kim loại + NO2 + O2
4Fe(NO3)2 → 2Fe2O3 + 8NO2+ O2
Câu 9. Khi nhiệt phân hoàn toàn muối nitrat của kim loại hóa trị I thu được 32,4 gam kim loại và 10,08 lít khí (đktc). Công thức của muối nitrat đó là.
A. AgNO3
B. NaNO3
C. KNO3
D. LiNO3
Hướng dẫn giải
Đáp án A
Gọi kim loại cần tìm là M ⇒ muối nitrat là: MNO3
MNO3 → M + NO2+ 1/2 O2
a → a → a → a/2
a+ a/2 = 1,5a = 10,08/22,4 = 0,45 ⇒ a = 0,3
M = 32,4/0,3 = 108 ⇒ M là Ag
Câu 10. Nhúng thanh Al vào dung dịch HNO3 loãng, không thấy có khí thoát ra. Kết luận nào sao đây là đúng:
A. Al không phản ứng với dung dịch HNO3 loãng
B. Al bị thụ động hóa trong dung dịch HNO3 loãng
C. Al phản ứng với HNO3 tạo ra muối amoni
D. Al phản ứng với HNO3 tạo ra muối và nước
Hướng dẫn giải
Đáp án C
Phương trình phản ứng Al tác dụng với HNO3 loãng ra NH4NO3
8Al + 30HNO3 → 8Al(NO3)3 + 3NH4NO3+ 9H2O