Phản ứng thế trong nghiên cứu hóa học được định nghĩa như như thế nào? Ví dụ về các phản ứng thế cùng với bài tập thực hành? Tất cả sẽ có ngay trong bài viết tổng hợp của chúng tôi dưới đây.
Mục lục bài viết
1. Phản ứng thế là gì?
Tại bài số 33, sách giáo khoa hóa học 8 thì phản ứng thế được định nghĩa rất rõ ràng, chi tiết và cụ thể. Theo đó: “Phản ứng thế là phản ứng hóa học giữa đơn chất và hợp chất, trong đó nguyên tử của đơn chất thay thế nguyên tử của một nguyên tố khác trong hợp chất”.
2. Phân loại phản ứng thế:
Khi đề cập đến phản ứng thế, ta nhắc đến phản ứng thế trong hóa học hữu cơ và phản ứng thế trong hóa học vô cơ.
Phản ứng thế trong hóa học vô cơ
Phản ứng thế trong hóa học vô cơ luôn xuất hiện sự thay đổi số oxi hóa của các nguyên tố. Tính chất đặc trưng, cốt lõi nhất của phản ứng thế là một phản ứng hóa học, trong đó một nguyên tố có hoạt động hóa học mạnh hơn sẽ thay thế cho các nguyên tố có hoạt động hóa học yếu hơn trong các hợp chất của nguyên tố này, trong các điều kiện cụ thể, nhất định về cả nhiệt độ và áp suất.
Phương trình phản ứng minh họa: A + BX -> AX + B
Trong chương trình hóa học tại cấp học phổ thông, các nhà khoa học thường hay đề cập đến dãy Beketop, đây sẽ là dãy được sử dụng trong việc so sánh độ hoạt động hóa học của một số kim loại với nhau và cùng với đó là so với hiđro. Mặc dù vậy thì dãy này chỉ thể hiện cho một số loại kim loại điển hình ở điều kiện tiêu chuẩn. Trong thực tế, ở nhiệt độ cao thì một số phi kim như cacbon có khả năng thế chỗ của kim loại trong hợp chất của nó. Đơn cử như phản ứng khử oxit sắt (III) là một phản ứng thế điển hình: (3C + Fe_2O_3 rightarrow 3CO + 2Fe)Dãy hoạt động hóa học (dãy beketop):
Phản ứng thế trong hóa học hữu cơ
Phản ứng thế trong các hợp chất hữu cơ tiếp tục được phân loại nhỏ hơn thành 3 loại chính, đó là:
- Phản ứng thế ái lực điện tử.
- Phản ứng thế ái lực hạt nhân.
- Phản ứng thế gốc.
Đây là một phản ứng tiêu biểu, thường xuất hiện ở các hydrocacbon no, ký hiệu là S. Đây là hình thức phản ứng dây chuyền và muốn khơi mào làm xuất hiện phản ứng, chúng ta cần phải chiếu sáng hoặc cho thêm các chất dễ phân hủy thành gốc tự do hoạt động vào.
Lưu ý:
Phản ứng này thường gặp ở các hiđrocacbon no, được ký hiệu là S. Phản ứng thế halogen trong các phân tử ankan sẽ xảy ra theo cơ chế gốc (cơ chế SR). Đây là một phản ứng mang tính chất dây chuyền. Do đó, muốn khơi mào phản ứng, cần phải chiếu sáng hoặc thêm các chất dễ phân hủy thành gốc tự do hoạt động vào.
Ví dụ: Xét quá trình phản ứng giữa metan và clo, phản ứng xảy ra theo cơ chế gốc, trải qua 3 giai đoạn: khơi mào, phát triển mạch, tắt mạch.
- Khơi mào:
- Cl2→Cl′+Cl′ (điều kiện: ánh sáng khuếch tán).
- Phát triển mạch:
- CH4+Cl′→CH′3+HCl
- CH′3+Cl2→CH3Cl+Cl′
- Tắt mạch:
- Cl′+Cl′→Cl2
- CH′3+Cl′→CH3Cl
- CH′3+CH′3→CH3−CH3
3. Một số ví dụ về phản ứng thế thường gặp:
Trong hóa học vô cơ
Fe+HCl→FeCl2+H2
3 Cl2+2 NH3→6 HCl+N2
Zn+CuCl2→Cu+ZnCl2
2 Al+6 HCl→2 AlCl3+3 H22
HCl + Zn → H2 + ZnCl2
2 C + SiO2 → 2CO + Si
Fe + CuCl2 → Cu + FeCl2
Fe + H2SO4→H2 + FeSO4
2 AlCl3 + 3 Mg→2 A l+ 3 MgCl2
3 Cl2 + 6 Fe(NO3)2→4 Fe(NO3)3 + 2 FeCl3
4. Cách thức điều chế hidro trong phản ứng thế
4.1. Điều chế khí hidro trong phòng thí nghiệm
– Trong phòng thí nghiệm, người ta điều chế khí hidro bằng cách cho axit (HCl, H2SO4 loãng,…) tác dụng với kim loại (Zn, Fe, Al,…).
Chi tiết quy trình điều chế như sau:
- Cho một mảnh kẽm hoặc từ hai đến ba hạt kẽm (Zn) vào trong ống nghiệm.
- Rót hai đến ba ml dung dịch axit clohidric (HCl) vào trong ống nghiệm đó.
- Thực hiện việc đậy ống nghiệm lại trông qua một nút cao su có ống dẫn khí xuyên qua. Sau khi khử độ tinh khiết, chắc chắn dòng khí hidro không có lẫn khí oxi. Lúc này, chúng ta tiến hành đưa que đom đóm vẫn còn tàn đỏ vào đầu ống dẫn khí và thấy que đóm bắt đầu cháy.
- Tiếp tục nhỏ tiếp một giọt dung dịch trong ống nghiệm lên bên trên mặt kính đồng hồ và đem cô cạn quan sát hiện tượng, chúng ta có thể thấy được rằng
- Xuất hiện các bọt khí trên bề mặt mảnh kẽm rồi thoát ra khỏi chất lỏng rồi tiếp theo đó mảnh kẽm tan dần.
- Que đóm đóm còn tàn đỏ được đưa vào đầu ống dẫn khí, khí thoát ra không còn khiến cho than hồng bùng cháy nữa.
- Khi đưa que đóm đang cháy vào đầu ống dẫn khí, khí thoát ra sẽ vẫn tiếp tục cháy được trong không khí với ngọn lửa có màu xanh nhạt và đó khí hidro.
- Tiến hành cô cạn một giọt dung dịch, ta sẽ thu được một chất rắn màu trắng đó là kẽm clorua (ZnCl2).
Ta có phương trình hóa học điều chế Hidro trong phòng thí nghiệm như sau:
Lưu ý: Có thể thay thế HCl bằng H2SO4 loãng; Zn bằng Fe hoặc Al.
Trường hợp muốn điều chế hidro trong phòng thí nghiệm để thu lại được lượng lớn hơn, ta có thể thực hiện theo các bước như sau:
Đổ dung dịch axit HCl loãng vào phễu.
Mở khóa cho dung dịch axit từ phễu chảy xuống lọ và tác dụng với kẽm.
Thu khí hiđro vào ống nghiệm bằng cách: Hiđro đẩy nước ra khỏi ống nghiệm hoặc hiđro đẩy không khí ra khỏi ống nghiệm.
Một số phản ứng được ứng dụng khi điều chế khí H2 trong phòng thí nghiệm:
Zn + 2HCl → ZnCl2 + H2
Fe + 2HCl → FeCl2 + H2
2Al + 6HCl → 2AlCl3 + 3H2
Fe + H2SO4 → FeSO4 + H2
4.2. Điều chế khí hidro trong công nghiệp
Trong công nghiệp, những phương pháp điều chế khí hidro là:
Điện phân nước
Dùng than khử oxi của H2O trong lò khí than
Điều chế từ khí tự nhiên, khí dầu mỏ
5. Một số bài tập thực hành về phản ứng thế.
Dạng 1: Phản ứng thế halogen của ankan
Phản ứng halogen hóa Ankan là một dạng phản ứng một hay nhiều nguyên tử H bị thay thế bởi một hay nhiều nguyên tử Halogen. Căn cứ vào thành phần phần trăm khối lượng, khối lượng mol của sản phẩm hoặc khối lượng mol trung bình của hỗn hợp sản phẩm để xác định Hidrocacbon
CnH2n+2 + aX2 → CnH2n+2-aXa +aHX
Phương pháp giải bài tập thế halogen
– Bước 1: Viết phương trình phản ứng của ankan với Cl2 hoặc Br2. Nếu đề bài không đưa ra dữ kiện sản phẩm thế là monohalogen, đihalogen,… thì ta phải khái quát hóa phản ứng
– Bước 2: Tính khối lượng mol của sản phẩm thế hoặc khối lượng mol trung bình của hỗn hợp sản phẩm để tìm ra số nguyên tử cacbon trong ankan hoặc mối liên hệ giữa số cacbon và số nguyên tử clo, brom trong sản phẩm thế. Qua đó ta sẽ xác định được số nguyên tử cacbon cũng như số nguyên tử clo, brom trong sản phẩm thế. Từ đó tìm được công thức cấu tạo của ankan ban đầu cũng như công thức cấu tạo của các sản phẩm thế.
Ví dụ minh họa
Bài 1: Một ankan A có thành phần phần trăm C là 83,33%. Tìm CTPT và xác định CTCT đúng của A biết rằng khi cho A tác dụng với Cl2 theo tỉ lệ mol 1: 1 ta chỉ thu được 1 sản phẩm thế monoclo.
Hướng dẫn:
Gọi CTPT của ankan là: CnH2n+2
%(m)C = 12n/(12n+2n+2).100% = 83,33%
⇒ n = 5. Vậy CTPT của A là C5H12
A tác dụng với Cl2 theo tỉ lệ mol 1: 1 ta chỉ thu được 1 sản phẩm thế monoclo.
⇒ CTCT đúng của A là:
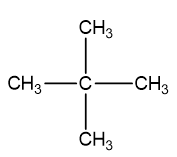
Bài 2: Clo hóa ankan X theo tỉ lệ mol 1:1 tạo sản phẩm dẫn xuất monoclo có thành phần khối lượng Clo là 45,223%. Vậy công thức phân tử của X là gì?
Hướng dẫn chi tiết cách giải:
Ta có: CnH2n+2 + Cl2 → CnH2n+1Cl + HCl
⇒ 35,5 / (14n + 36,5) . 100 = 45,223 => n = 3
Vậy ta có công thức phân tử của X là: C3H8
Dạng 2: Bài tập phản ứng thế hidrocacbon
Bài 1: Hai xicloankan N và M đều có tỉ khối hơi khi so sánh với metan bằng 5,25. Khi tham gia phản ứng thế clo (ánh sáng, tỉ lệ mol 1:1) N cho 1 sản phẩm thế còn M cho 4 sản phẩm thế. Tên gọi của các xicloankan N và M là ?
Hướng dẫn cách giải chi tiết
Cả 2 xicloanan đều có tỷ khối hơi so với metan bằng 5,25 => Công thức phân tử chính là C6H12
N cho ra duy nhất 1 đồng phân => N buộc phải là là xiclohexan => Loại A và D
M cho ra 4 đồng phân => M chỉ có thể là metyl xiclopentan
Câu 2: TNT (2,4,6- trinitrotoluen) được điều chế trong điều kiện đun nóng thông qua phản ứng của toluen với hỗn hợp gồm HNO3 đặc và H2SO4 đặc. Biết hiệu suất của toàn bộ quá trình tổng hợp là 80%. Tính lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluene?
Số mol toluene tham gia phản ứng: ntoluen = 230/94 = 2,5 mol
Phương trình phản ứng:
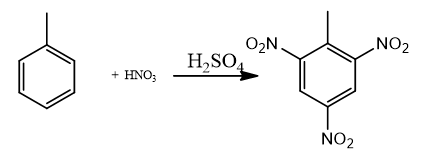
Lượng TNT (2,4,6- trinitrotoluen) tạo thành từ 230 gam toluene:
mTNT = 2,5.227.80/100 = 454 gam




