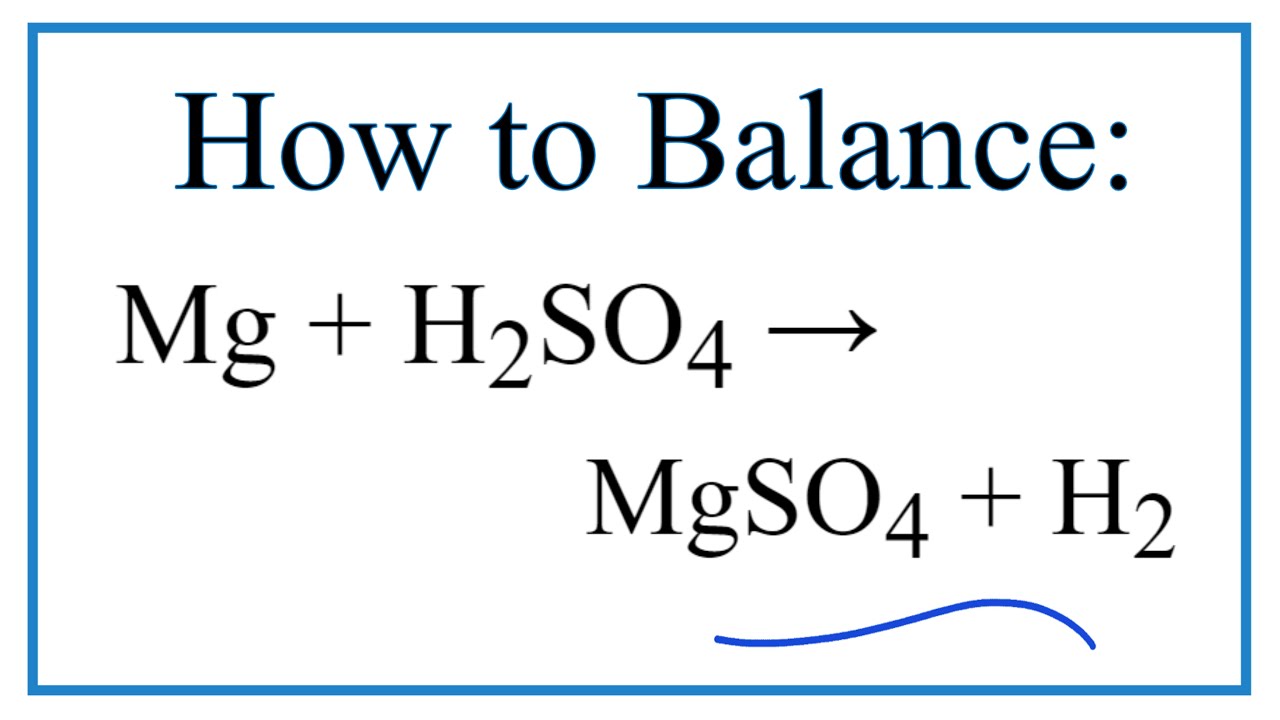
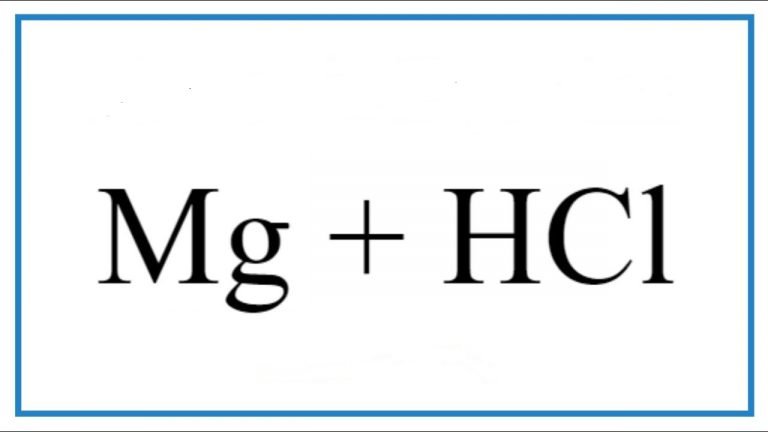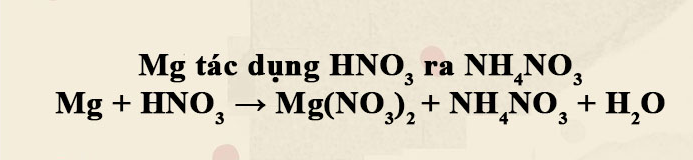Phản ứng trên là phản ứng oxi-hoá khử trong đó sắt trong Fe3O4 bị khử thành FeCl2 trong khi HCl oxi hóa thành FeCl3 và H2O. Phản ứng này còn được gọi là phản ứng khử kim loại. Mời bạn đọc tham khảo dưới đây.
Mục lục bài viết
1. Phương trình phản ứng Fe3O4 ra FeCl3:
Phương trình phản ứng Fe3O4 tác dụng với dung dịch axit HCl là phương trình hóa học đơn giản, nhưng lại rất quan trọng bởi vai trò của nó trong các ứng dụng thực tiễn. Phản ứng này được sử dụng trong nhiều lĩnh vực khác nhau, như công nghiệp, y học, môi trường, v.v.
Phương trình phản ứng Fe3O4 tác dụng với dung dịch axit HCl được phát biểu như sau:
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
1.1. Điều kiện phản ứng Fe3O4+ HCl:
Nhiệt độ là một trong những yếu tố quan trọng ảnh hưởng đến tốc độ phản ứng Fe3O4 tác dụng với dung dịch axit HCl. Khi nhiệt độ tăng lên, phản ứng diễn ra nhanh hơn do tốc độ phản ứng tăng lên. Tuy nhiên, quá trình phản ứng cũng có thể bị ảnh hưởng nếu nhiệt độ quá cao và vượt quá giới hạn chịu nhiệt của các tác nhân hóa học.
Ngoài ra, nồng độ dung dịch axit HCl cũng là một trong những yếu tố quan trọng ảnh hưởng đến tốc độ phản ứng Fe3O4 tác dụng với dung dịch axit. Khi nồng độ dung dịch tăng lên thì tốc độ phản ứng cũng tăng lên theo.
1.2. Cách thực hiện phản ứng Fe3O4 HCl:
Các bước thực hiện phản ứng Fe3O4 tác dụng với dung dịch axit HCl như sau:
Chuẩn bị ống nghiệm, cho Fe3O4 vào bên trong.
Nhỏ từ từ dung dịch axit HCl vào ống nghiệm đã bỏ sẵn Fe3O4. Để đảm bảo an toàn, cần đeo kính bảo vệ và làm việc trong không khí thoáng mát.
Sử dụng cặp kẹp ống nghiệm để lắc nhẹ và đều hỗn hợp trong ống.
Đun nóng ống nghiệm lên trên ngọn lửa đèn cồn.
Tiếp tục lắc đều và đun nóng cho đến khi phản ứng hoàn toàn diễn ra. Khi đó, ta có thể quan sát thấy sự thay đổi màu sắc và hình dạng của hỗn hợp.
Việc thực hiện các bước này sẽ giúp phản ứng diễn ra hiệu quả và đạt được kết quả tốt nhất. Ngoài ra, cần lưu ý về an toàn khi thực hiện phản ứng này, đặc biệt là khi sử dụng dung dịch axit HCl. Cần đeo kính bảo vệ và làm việc trong không khí thoáng mát để đảm bảo an toàn cho bản thân và những người xung quanh.
2. Hiện tượng sau phản ứng Fe3O4 tác dụng HCl:
Khi hợp chất Fe3O4 tác dụng với axit clohidric (HCl), phản ứng sẽ tạo ra một sản phẩm mới gọi là muối, có thể được tách ra từ hỗn hợp ban đầu bằng phương pháp kết tủa. Ngoài ra, phản ứng này còn sinh ra khí hidro (H2) và nhiệt nữa. Quá trình này có thể được mô tả như sau: trước tiên, Fe3O4 hòa tan trong dung dịch axit, giải phóng ion sắt (Fe2+) và ion oxit clo (Cl-); sau đó, ion sắt sẽ tương tác với H+ để tạo thành khí hidro, trong khi ion clo kết hợp với ion sắt để tạo ra sản phẩm muối. Việc tách muối ra khỏi dung dịch có thể được thực hiện bằng cách sử dụng phương pháp kết tủa, trong đó một chất pH được sử dụng để thay đổi độ acid của dung dịch và kết tủa muối. Tuy nhiên, quá trình này có thể bị ảnh hưởng bởi nhiều yếu tố, bao gồm nhiệt độ, lượng phản ứng và chất lượng của các chất tham gia.
3. Tính chất hóa học của Fe3O4:
Fe3O4 là một hợp chất quan trọng của sắt và oxit. Nó được tìm thấy nhiều trong quặng manhetit và có tính từ tính. Công thức phân tử của Fe3O4 là FeO.Fe2O3. Fe3O4 có tính chất hóa học đa dạng và được sử dụng trong nhiều ứng dụng khác nhau.
3.1. Tính chất vật lý:
Fe3O4 là một chất rắn màu đen, không tan trong nước và có tính từ tính mạnh. Vì tính từ tính này, nó được sử dụng trong nhiều ứng dụng từ tính, chẳng hạn như trong sản xuất nam châm.
3.2. Tính chất hóa học:
Fe3O4 có tính oxi hóa và khử. Khi phản ứng với axit như HCl và H2SO4 loãng, nó tạo ra hỗn hợp muối sắt (II) và sắt (III). Khi tiếp xúc với các chất có tính oxi hóa mạnh, Fe3O4 sẽ tác dụng như một chất khử. Khi tác dụng với các chất khử mạnh ở nhiệt độ cao như H2, CO và Al, Fe3O4 sẽ tác dụng như một chất oxi hóa.
Fe3O4 cũng được sử dụng trong xử lý nước thải và sản xuất mực in. Ngoài ra, Fe3O4 còn có ứng dụng trong y tế để điều trị ung thư và hình thành hình ảnh y tế. Fe3O4 cũng được sử dụng trong các ứng dụng từ tính khác nhau, chẳng hạn như trong sản xuất thiết bị điện tử và các thiết bị y tế như máy siêu âm.
Vì những tính chất đa dạng của Fe3O4, nó là một hợp chất quan trọng của sắt và oxit và có nhiều ứng dụng trong nhiều lĩnh vực khác nhau.
4. Bài tập vận dụng liên quan:
Câu 1. Cho m gam bột Zn vào 500 ml dung dịch Fe2(SO4)3 0,24M. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng dung dịch tăng thêm 9,6 gam so với khối lượng dung dịch ban đầu. Giá trị của m là
A. 29,25.
B. 48,75.
C. 32,50.
D. 28,80.
Đáp án D
nFe2(SO4)3= 0,24.0,5 = 0,12mol
nFe3+= 0,24
Zn + 2Fe3+ → Zn2+ + 2Fe2+
0,12….0,24…………….0,24
Zn + Fe2+ → Zn2+ + Fe
x……………………x
→ mdd tăng= mZn – mFe= 65(0,12 + x) – 56x = 9,6 → x = 0,2
=> nZn ban đầu = 0,12 + 0,2 = 0,23 mol => mZn= 0,32.65 = 28,8 gam
Câu 2. Phản ứng xảy ra khi đốt cháy sắt trong không khí là
A. 3Fe + 2O2 → Fe3O4.
B. 4Fe + 3O2 → 2Fe2O3.
C. 2Fe + O2 → 2FeO.
D. tạo hỗn hợp FeO, Fe2O3, Fe3O4.
Đáp án A
Phản ứng xảy ra khi đốt cháy sắt trong không khí là
3Fe + 2O2 → Fe3O4.
Câu 3. Cho các phản ứng sau:
(1) Fe(OH)2 + H2SO4 đặc →
(2) Fe + H2SO4 loãng →
(3) Fe(OH)3 + H2SO4 đặc →
(4) Fe3O4 + H2SO4 loãng →
(5) Cu + H2SO4 loãng + dd NaNO3 →
(6) FeCO3 + H2SO4 đặc →
Số phản ứng hóa học trong đó H2SO4 đóng vai trò là chất oxi hóa là:
A. 2
B. 4
C. 3
D. 5
Đáp án C
Các phản ứng : (1) , (2) , (6)
(1) 8Fe(OH)2 + 13H2SO4 đặc → 4Fe2(SO4)3 + H2S + 20H2O
(2) Fe + H2SO4 loãng → FeSO4 + H2
(3) 2 Fe(OH)3 + 3 H2SO4 → Fe2(SO4)3 + 6 H2O
(4) Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
(5) Cu + 4H2SO4 + 2NaNO3⟶ 3CuSO4 + Na2SO4 + 2NO + 4H2O
(6) 2FeCO3 + 4H2SO4→ Fe2(SO4)3+ SO2 + 2CO2 + 4H2O
Câu 4. Nhận xét nào sau đây không đúng
A. Trong dung dịch Fe khử được ion Cu2+ thành Cu.
B. Bột nhôm bốc cháy khi gặp khí clo.
C. Các kim loại Na, K, Ba đều phản ứng với nước ở điều kiện thường.
D. Fe phản ứng với dung dịch HCl hay phản ứng với Clo đều tạo thành một loại muối.
Đáp án D
Fe phản ứng với dung dịch HCl hay phản ứng với Clo đều tạo thành một loại muối.
Phương trình phản ứng minh họa
Fe + 2HCl → FeCl2 + H2↑
2Fe + 3Cl2→ 2FeCl3 ⇒ thu được 2 loại muối.
Câu 5. Cho dung dịch NaOH đến dư vào dung dịch FeCl2 thấy xuất hiện kết tủa
A. trắng xanh, sau đó chuyển nâu đỏ.
B. keo trắng, sau đó tan dần.
C. keo trắng không tan.
D. nâu đỏ
Đáp án A
Ban đầu tạo Fe(OH)2 có màu trắng xanh:
FeCl2 + 2NaOH → Fe(OH)2 (trắng xanh) + 2NaCl
Sau đó Fe(OH)2 bị O2 (trong dung dịch và không khí) oxi hóa thành Fe(OH)3 có màu nâu đỏ:
Fe(OH)2 + 1/4O2 + 1/2H2O → Fe(OH)3(nâu đỏ)
Vậy hiện tượng là tạo kết tủa trắng xanh, sau đó chuyển nâu đỏ.
Câu 6. Cho Zn dư vào dung dịch AgNO3, Cu(NO3)2, Fe(NO3)3. Số phản ứng hoá học xảy ra là:
A. 1.
B. 2.
C. 3.
D. 4
Đáp án D
Phương trình phản ứng minh họa
Zn + 2AgNO3 → Zn(NO3)2 + 2Ag
Zn + 2Fe(NO3)3 → Zn(NO3)2+ 2Fe(NO3)2
Zn + Cu(NO3)2 → Zn(NO3)2+ Cu
Zn + Fe(NO3)2 → Zn(NO3)2+ Fe
Câu 7. Hòa tan Fe3O4 vào dung dịch HCl dư, thu được dung dịch X. Cho dãy các chất: KMnO4; Cl2; KOH; Na2CO3; CuSO4, HNO3; Fe; NaNO3. Số chất trong dãy tác dụng được với dung dịch X là
A. 7
B. 5
C. 4
D. 6
Đáp án A
Fe3O4 + HCl dư → dung dịch X gồm: FeCl2; FeCl3; HCl dư.
Vậy dung dịch X tác dụng được với các chất là: KMnO4; Cl2; KOH; Na2CO3; HNO3; Fe; NaNO3
Phương trình phản ứng minh họa
5FeCl2+ KMnO4 + 8HCl → 5FeCl3 + KCl + MnO2↓ + Cl2↑ + 4H2O
2FeCl2 + Cl2 → 2FeCl3
FeCl2 + KOH → Fe(OH)2↓ + 2KCl
FeCl3 + KOH → Fe(OH)3↓ + 3KCl
HCl + KOH → KCl + H2O
2FeCl3 + 3Na2CO3 + 3H2O → 2Fe(OH)3↓ + 3CO2↑ + 6NaCl
2HCl + Na2CO3 → 2NaCl + H2O + CO2↑
FeCl2+ 4HNO3 → Fe(NO3)3 + 2HCl + NO2 ↑ + H2O
2FeCl3 + Fe → 3FeCl2
2HCl + Fe → FeCl2 + H2↑
3Fe2+ + NO3- + 4H+ → 3Fe3+ + NO + 2H2O
=> vậy có tất cả 7 chất phản ứng với dd X
Câu 8. Cho 23,2 gam Fe3O4 tác dụng với dung dịch HCl dư thu được muối sắt có khối lượng là:
A. 48,6 gam
B. 28,9 gam
C. 45,2 gam
D. 25,4 gam
Đáp án C
nFe3O4 = 23,2: 232 = 0,1 mol
Phương trình phản ứng minh họa
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O
Mol 0,1 → 0,1 → 0,2
mmuối = mFeCl2 + mFeCl3 = 0,1.127 + 0,2.162,5 = 45,2g
Câu 9. Cho 2,24 gam Fe tác dụng với oxi, thu được 3,04 gam hỗn hợp X gồm 2 oxit. Để hoà tan hết X cần thể tích dung dịch HCl 2M là
A. 25 ml.
B. 50 ml.
C. 100 ml.
D. 150 ml.
Đáp án B
Áp dụng bảo toàn nguyên tố (mol nguyên tử)
Oxit + HCl → muối clorua + H2O
nHCl = nH = 2.nO =
VddHCl2M = 0,1.1000/2 = 50ml
Câu 10. Cho dung dịch NaOH dư vào dung dịch chứa FeCl2 và FeCl3, thu được kết tủa X. Nung X trong không khí đến khối lượng không đổi, thu được chất rắn là
A. FeO.
B. FeO và Fe2O3.
C. Fe3O4.
D. Fe2O3.
Đáp án D
Phương trình phản ứng xảy ra
FeCl2 + NaOH → Fe(OH)2 + NaCl
FeCl3 + NaOH → Fe(OH)3 + NaCl
X gồm Fe(OH)2 và Fe(OH)3. Nung X ngoài không khí thu được Fe2O3:
Fe(OH)2 + O2 → Fe2O3 + H2O
Fe(OH)3 → Fe2O3 + H2O
Câu 11. Dãy các chất và dung dịch nào sau đây khi lấy dư có thể oxi hoá Fe thành Fe (III)?
A. HCl, HNO3 đặc, nóng, H2SO4 đặc, nóng
B. Cl2, HNO3 nóng, H2SO4 đặc, nguội
C. bột lưu huỳnh, H2SO4 đặc, nóng, HCl
D. Cl2, Cu(NO3)2, HNO3 loãng
Đáp án D
Phương trình phản ứng minh họa
2Fe + 3Cl2 → 2FeCl3
2Fe + 3Cu(NO3)2 →2Fe(NO3)3 + 3Cu
Fe + 4HNO3 loãng → Fe(NO3)3 + NO + 2H2O
Câu 12. Hòa tan hoàn toàn 5,6 gam hỗn hợp FeO, Fe2O3 và Fe3O4 cần vừa đủ V ml dung dịch HCl 1M , thu được dung dịch X. Cho từ từ dung dịch NaOH dư vào dung dịch X thu được kết tủa Y. Nung Y trong không khí đến khối lượng không đổi thu được 6 gam chất rắn. Tính V ?
A. 87,5ml
B. 125ml
C. 62,5ml
D. 175 ml
Đáp án D
Quy đổi thành 5,6 gam ( Fe : x mol và O : y mol )
Sơ đồ hợp thức: 2Fe → Fe2O3
Ta có: nFe = 2nFe2O3 = 2 . 6/160 = 0,075 mol
=> nO (oxit) = ( 5,6 – 0,075.56 )/16 = 0,0875 mol
=> nHCl p/u = 2 nO (oxit) = 0,175 mol
=> V = 175 ml
Câu 13. Dung dịch X gồm 0,2 mol HCl và 0,025 mol Cu(NO3)2. Cho m gam bột Fe vào dung dịch, khuấy đều cho đến khi phản ứng kết thúc thu được chất rắn Z gồm hai kim loại có khối lượng 0,4m gam. Giả sử sản phẩm khử HNO3 duy nhất chỉ có NO. Giá trị của m bằng:
A. 20 gam
B. 30 gam
C. 40 gam
D. 50 gam
Đáp án A
Sau phản ứng thu được hỗn hợp gồm 2 kim loại Fe, Cu → H+ và NO3-, Cu2+ hết.
Dung dịch chỉ chứa FeCl2: 0,1 mol (bảo toàn Cl- = 0,2 mol), Cu: 0,025 mol
⇒ Khối lượng Fe phản ứng là: mFe pư = 0,1. 56 = 5,6 gam
→ 0,4m gam kim loại gồm Fe dư: m – 5,6 (gam) và Cu: 0,025. 64 = 1,6 gam
→ 0,4m = 1,6 + m – 0,1.56 → m = 20 gam.
Câu 14. Thổi hỗn hợp khí CO và H2 đi qua a gam hỗn hợp gồm CuO và Fe3O4 có tỉ lệ mol 1:2, sau phản ứng thu được b gam chất rắn X. Hòa tan hoàn toàn b gam X bằng dung dịch HNO3 loãng dư, thu được dung dịch Y (không chứa ion Fe2+). Cô cạn dung dịch Y thu được 82 gam muối khan. Giá trị của a là
A. 27,2.
B. 10,6.
C. 12,8.
D. 13,6.
Đáp án A
nCu= x mol;
nFe3O4 = 2x mol;
→ nCu(NO3)2 = x; nFe(NO3)3 = 6x mol
mmuối= mCu(NO3)2 + mFe(NO3)3 → 188x + 242.6x = 82 → x = 0,05 mol
→ x = 0,05.80 + 0,05.2.232 = 27,2 gam.
Câu 15. Những nhận định sau về kim loại sắt:
(1) Kim loại sắt có tính khử trung bình.
(2) Ion Fe2+ bền hơn Fe3+.
(3) Fe bị thụ động trong H2SO4 đặc nguội.
(4) Quặng manhetit là quặng có hàm lượng sắt cao nhất.
(5) Trái đất tự quay và sắt là nguyên nhân làm Trái Đất có từ tính.
(6) Kim loại sắt có thể khử được ion Fe3+.
Số nhận định đúng là
A. 3
B. 4
C. 5
D. 6
Đáp án B
(1) đúng
(2) sai, Fe2+ trong không khí dễ bị oxi hóa thành Fe3+
(3) đúng
(4) đúng, quặng manhetit (Fe3O4) là quặng có hàm lượng Fe cao nhất.
(5) sai, vì từ trường Trái Đất sinh ra do sự chuyển động của các chất lỏng dẫn điện
(6) đúng, Fe + 2Fe3+ → 3Fe2+
Vậy có 4 phát biểu đúng
Câu 16. Ngâm thanh Cu (dư) vào dung dịch AgNO3 thu được dung dịch X. Sau đó ngâm thanh Fe (dư) vào dung dịch X thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y có chứa chất tan là:
A. Fe(NO3)3.
B. Fe(NO3)2.
C. Fe(NO3)2, Cu(NO3)2
D. Fe(NO3)3, Fe(NO3)2.
Đáp án B
Các phản ứng xảy ra:
Cu (dư) + AgNO3 → Cu(NO3)2 + Ag
Cu(NO3)2 + Fe(dư) → Fe(NO3)2+ Cu
Vậy dung dịch Y chứa Fe(NO3)2.
Câu 17. Có 4 dung dịch đựng riêng biệt: (a) HCl; (b) CuCl2; (c) FeCl2; (d) HCl có lẫn CuCl2. Nhúng vào mỗi dung dịch một thanh sắt nguyên chất. Số trường hợp xảy ra ăn mòn điện hóa là
A. 0
B. 1
C. 3
D. 2
Đáp án D
Để xảy ra quá trình ăn mòn điện hóa cần thỏa mãn 3 điều kiện:
+ Có 2 điện cực khác bản
+ 2 điện cực tiếp xúc trực tiếp hoặc gián tiếp với nhau
+ 2 điện cực được nhúng trong cùng 1 dung dịch chất điện li
Có 2 trường hợp thỏa mãn: Fe nhúng vào dung dịch CuCl2 và Fe nhúng vào dung dịch CuCl2 + HCl
Câu 18. Kim loại sắt phản ứng với lượng dư dung dịch chất nào sau đây tạo ra muối sắt(II)?
A. H2SO4 đặc, nóng.
B. HNO3 loãng.
C. H2SO4 loãng.
D. HNO3 đặc nóng.
Đáp án C
Tác dụng với HNO3 dư (loãng hay đặc nóng) đều cho muối Fe3+
Tác dụng với H2SO4 đặc nóng cho Fe3+; tác dụng với H2SO4 loãng cho Fe2+
Fe + H2SO4 loãng → FeSO4 + H2
Câu 19. Cho các nội dung nhận định sau:
(a) Tính chất hoá học đặc trưng của kim loại là tính khử.
(b) Đồng (Cu) không khử được muối sắt (III) (Fe3+).
(c) Ăn mòn kim loại là một quá trình hoá học trong đó kim loại bị ăn mòn bởi các axit trong môi trường không khí.
(d) Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm.
Số nhận định đúng là
A. 2.
B. 3.
C. 4.
D. 1.
Đáp án A
(a) Đúng Tính chất hoá học đặc trưng của kim loại là tính khử.
(b) Sai vì Đồng (Cu) khử được muối sắt (III) (Fe3+).
Phản ứng minh họa
Cu + FeCl3 → CuCl2 + FeCl2
(c) Sai vì “Ăn mòn kim loại” là sự phá hủy kim loại do tác dụng hóa học của môi trường xung quanh.
(d) Đúng Để bảo vệ vỏ tàu biển làm bằng thép, người ta gắn vào mặt ngoài vỏ tàu (phần chìm trong nước biển) những khối kẽm.
Câu 20. Cho 5,68 gam hỗn hợp gồm Fe, FeO, Fe2O3 và Fe3O4 phản ứng hết với dung dịch HNO3 loãng dư, thu được 0,672 lít khí NO (sản phẩm khử duy nhất) (ở đktc) và dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m là:
A. 38,72
B. 35,50
C. 19,36
D. 34,36
Đáp án C
Xem hỗn hợp Fe, FeO, Fe2O3 và Fe3O4 chỉ gồm 2 nguyên tố Fe và O
Ta có sơ đồ: Fe: a mol; Fe(NO3)3: a mol
O: b mol
Ta có 56x + 16y = 5,68 (1)
Quá trình nhường electron:
Fe0 – 3e → Fe+3
a → 3a
Quá trình nhận electron:
O+0 + 2e → O-2
b → 2b
N+5 + 3e → N+2
0,09 0,03
Áp dụng định luật bảo toàn electron, ta có: 3a = 2b + 0,09 (2)
Từ (1) và (2) → x = 0,09 mol và y = 0,075 mol
⇒ mFe(NO3)3 = 0,08. 242 = 19,36 (g)