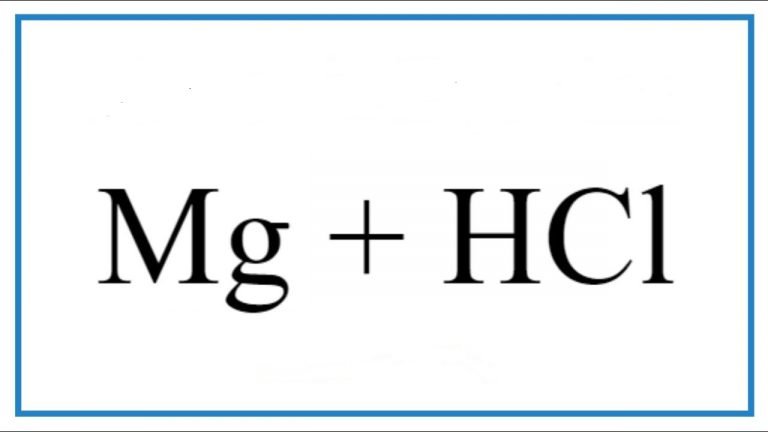Trong phản ứng này, sắt (Fe) bị oxi hóa thành ion Fe2+ còn axit clohidric (HCl) bị khử thành khí hiđro (H2). Công thức hóa học của sản phẩm clorua sắt (FeCl2) cho biết rằng một nguyên tử sắt (Fe) đã kết hợp với hai nguyên tử clo (Cl) để tạo thành phân tử FeCl2.
Mục lục bài viết
1. Tính chất của phản ứng Fe + HCl → FeCl2 + H2:
Phản ứng giữa sắt (Fe) và axit clohidric (HCl) tạo ra clorua sắt (FeCl2) và khí hiđro (H2) theo phương trình hóa học sau đây:
Fe + 2HCl → FeCl2 + H2
Trong phản ứng này, sắt (Fe) bị oxi hóa thành ion Fe2+ còn axit clohidric (HCl) bị khử thành khí hiđro (H2). Công thức hóa học của sản phẩm clorua sắt (FeCl2) cho biết rằng một nguyên tử sắt (Fe) đã kết hợp với hai nguyên tử clo (Cl) để tạo thành phân tử FeCl2.
Phản ứng giữa Fe và HCl là một ví dụ về phản ứng trao đổi. Trong phản ứng này, các nguyên tử và ion trao đổi để tạo ra sản phẩm khác với các chất ban đầu.
2. Điều kiện xảy ra phản ứng Fe + HCl → FeCl2 + H2:
Phản ứng giữa Fe (sắt) và HCl (axit clohidric) để tạo thành FeCl2 (clorua sắt II) và H2 (hidro) là một phản ứng oxi-hoá khử quan trọng trong hóa học. Tuy nhiên, để phản ứng này xảy ra, cần đáp ứng một số điều kiện nhất định.
Đầu tiên, nhiệt độ phải đủ cao để kích thích tốc độ phản ứng. Phản ứng này là một phản ứng exothermic (giải phóng nhiệt), nghĩa là nó sẽ tỏa ra nhiệt khi xảy ra. Tuy nhiên, phản ứng sẽ không xảy ra nếu nhiệt độ quá thấp. Vì vậy, cần đảm bảo rằng nhiệt độ đủ cao để kích thích phản ứng.
Thứ hai, phải có chất xúc tác để tăng tốc độ phản ứng. Trong trường hợp này, Cu (đồng) được sử dụng như một chất xúc tác để giúp tăng tốc độ phản ứng. Chất xúc tác là một chất có khả năng tăng tốc độ phản ứng mà không tham gia vào phản ứng.
Thứ ba, phải có đủ lượng chất tham gia để phản ứng xảy ra hoàn toàn. Nếu không đủ Fe hoặc HCl, phản ứng sẽ không xảy ra hoặc sẽ xảy ra không hoàn toàn. Vì vậy, cần đảm bảo rằng đủ lượng Fe và HCl có sẵn để phản ứng xảy ra hoàn toàn.
Cuối cùng, phải có không khí để oxy hóa Fe thành Fe (II) trước khi phản ứng xảy ra. Khi sắt (Fe) tiếp xúc với không khí, nó sẽ bị oxy hóa thành Fe (II), điều này sẽ tạo điều kiện cho phản ứng tiếp diễn.
Khi đáp ứng đủ các điều kiện trên, phản ứng sẽ xảy ra theo phương trình: Fe + 2HCl → FeCl2 + H2
3. Ứng dụng của phản ứng Fe + HCl → FeCl2 + H2:
Phản ứng giữa sắt (Fe) và axit clohidric (HCl) tạo ra sản phẩm là clorua sắt (II) (FeCl2) và khí hiđro (H2). Phản ứng này được sử dụng rộng rãi trong ngành công nghiệp và có nhiều ứng dụng trong cuộc sống hàng ngày của chúng ta.
3.1. Sản xuất clorua sắt (II):
Phản ứng Fe + HCl là một trong những phản ứng cơ bản để sản xuất clorua sắt (II) trong ngành công nghiệp hóa chất. Clorua sắt (II) là một chất rắn màu trắng hoặc xám, được sử dụng để sản xuất các sản phẩm như mực in, xử lý nước và sản xuất thuốc nhuộm. Bên cạnh đó, clorua sắt (II) còn được sử dụng để sản xuất các hợp chất hữu cơ, ví dụ như tetracloretilen và các chất hóa học khác. Từ clorua sắt (II), cũng có thể sản xuất clorua sắt (III) (FeCl3), một chất lỏng màu nâu đỏ được sử dụng để sản xuất các sản phẩm hóa học khác.
3.2. Sản xuất khí hiđro:
Phản ứng Fe + HCl cũng là một trong những phản ứng tạo ra khí hiđro. Khí hiđro là một khí không màu, không mùi và không vị, được sử dụng rộng rãi trong ngành công nghiệp để sản xuất ammonia, lọc dầu và sản xuất pin nhiên liệu. Khí hiđro cũng được sử dụng trong việc sản xuất thuốc trừ sâu, trong các quá trình sản xuất thép và trong các ứng dụng năng lượng tái tạo, như tạo ra nhiên liệu từ nước bằng cách sử dụng điện năng.
3.3. Điều chế hidro clorua:
Phản ứng Fe + HCl cũng được sử dụng để điều chế hidro clorua (HCl). Hidro clorua là một chất khí không màu, có mùi hắc hơi, được sử dụng để sản xuất các sản phẩm như thuốc trừ sâu, chất tẩy vàng và các sản phẩm hóa học khác. Ngoài ra, hidro clorua còn được sử dụng trong việc sản xuất axit clohidric (HCl), một chất lỏng màu vàng nhạt được sử dụng trong sản xuất thuốc, chất tẩy và các sản phẩm hóa học khác.
3.4. Sản xuất pin nhiên liệu:
Ngoài việc sản xuất khí hiđro, phản ứng Fe + HCl còn được sử dụng trong việc sản xuất pin nhiên liệu. Pin nhiên liệu là một loại pin có thể sản xuất điện năng từ nhiên liệu tái tạo như hidro hoặc etanol. Phản ứng Fe + HCl cung cấp nguồn khí hiđro cho quá trình sản xuất nhiên liệu từ hidro, giúp tạo ra một nguồn năng lượng sạch và bền vững.
Với các ứng dụng chính như vậy, phản ứng Fe + HCl đóng vai trò quan trọng trong ngành công nghiệp và trong cuộc sống hàng ngày của chúng ta. Các sản phẩm được sản xuất từ phản ứng này không chỉ đóng vai trò quan trọng trong cuộc sống hàng ngày của chúng ta, mà còn có tác động đến nhiều lĩnh vực khác nhau của cuộc sống, bao gồm công nghiệp, y tế và môi trường.
4. Bài tập về phản ứng Fe + HCl → FeCl2 + H2:
Câu 1. Để nhận biết sự có mặt của Fe trong hỗn hợp gồm Fe và Al có thể dùng dung dịch nào
A. NaOH.
B. HCl.
C. H2SO4 (loãng).
D. CuSO4
A. NaCl được dung làm muối ăn và bảo quản thực phẩm.
B. HCl tác dụng với sắt tạo ra muối sắt (III)
C. Axit HCl vừa có tính oxi hóa, vừa có tính khử.
D. Nhỏ dung dịch AgNO3 vào dung dịch HCl, có kết tủa trắng.
Câu 3. Kim loại tác dụng với dung dịch HCl và tác dụng với khí Cl2 đều thu được cùng một muối là
A. Fe
B. Zn
C. Cu
D. Ag
Câu 4. Trong phòng thí nghiệm có thể điều chế khí hidro clorua bằng cách
A. Cho NaCl tinh thể tác dụng với H2SO4 đặc, đun nóng.
B. Cho NaCl tinh thể tác dụng với HNO3 đặc, đun nóng.
C. Cho NaCl tinh thể tác dụng với H2SO4 loãng, đun nóng.
D. Cho NaCl tinh thể tác dụng với HNO3 loãng, đun nóng.
Câu 5. Cho 8,4 gam một kim loại hóa trị II phản ứng hết với dung dịch HCl dư, thu được 3,36 lít H2 (đktc). Kim loại đó là
A. Ca
B. Ba
C. Fe
D. Mg
Câu 6. Cho 8,85 gam hỗn hợp X gồm Al, Mg tác dụng với dung dịch HCl dư, thu được 8,96 lít H2 (đktc). Thành phần phần trăm khối lượng của Al trong X là
A. 69,23%
B. 54,24%
C. 45,76%
D. 51,92%
Câu 7. Sắt tác dụng với H2O ở nhiệt độ cao hơn 570oC thì tạo ra H2 và sản phẩm rắn là
A. FeO.
B. Fe3O4.
C. Fe2O3.
D. Fe(OH)2.
Câu 8. Hòa tan 10 gam hỗn hợp bột Fe và Fe2O3 bằng một lượng dung dịch HCl vừa đủ, thu được 1,12 lít hidro (đktc) và dd X. Cho dd X tác dụng với dd NaOH lấy dư. Lấy kết tủa thu được đem nung nóng trong không khí đến khối lượng không đổi thu được chất rắn Y. Khối lượng chất rắn Y là:
A. 16 gam.
B. 11,6 gam.
C. 12 gam.
D. 15 gam.
Câu 9. Có 4 kim loại X, Y, Z, T đứng sau Mg trong dãy hoạt động hoá học. Biết rằng:
X và Y tác dụng với dung dịch HCl giải phóng khí hidro.
Z và T không phản ứng với dung dịch HCl.
Y tác dụng với dung dịch muối của X và giải phóng X.
T tác dụng được với dung dịch muối của Z và giải phóng Z.
Hãy xác định thứ tự sắp xếp nào sau đây là đúng (theo chiều hoạt động hóa học giảm dần)
A. Y, T, Z, X
B. T, X, Y, Z
C. Y, X, T, Z
D. X, Y, Z, T
Câu 10. Khi điều chế FeCl2 bằng cách cho Fe tác dụng với dung dịch HCl. Để bảo quản dung dịch FeCl2 thu được không bị chuyển thành hợp chất sắt (III), người ta có thể cho thêm vào dung dịch
A. một lượng sắt dư .
B. một lượng kẽm dư.
C. một lượng HCl dư.
D. một lượng HNO3 dư.
Câu 11. Khử m gam Fe3O4 bằng khí H2 thu được hổn hợp X gồm Fe và FeO, hỗn hợp X tác dụng vừa hết với 1,5 lít dung dịch H2SO4 0,2M (loãng). Giá trị của m là
A. 46,4 gam.
B. 23,2 gam.
C. 11,6 gam.
D. 34,8 gam.
Câu 12.Tính chất vật lí nào dưới đây không phải là tính chất của Fe kim loại?
A. Kim loại nặng, khó nóng chảy.
B. Màu vàng nâu, cứng và giòn.
C. Dẫn điện và nhiệt tốt.
D. Có tính nhiễm từ.
Câu 13. Sục khí Clo vào lượng dung dịch NaOH ở nhiệt độ thường sản phẩm là
A. NaCl, NaClO2
B. NaCl, NaClO3
C. NaCl, NaClO
D. chỉ có NaCl
Câu 14. Chỉ sử dụng một hóa chất duy nhất, nhận biết 4 dung dịch mất nhãn sau: KNO3, Cu(NO3)2, AgNO3, Fe(NO3)3. Dung dịch đó là:
A. dung dịch NaOH
B. dung dịch NaCl
C. dung dịch HCl
D. đung dịch H2SO4
Đáp án A
Câu 15. Kim loại Fe không phản ứng được với
A. Dung dịch HCl
B. Dung dịch H2SO4 loãng
C. Dung dịch CuCl2
D. H2SO4 đặc, nguội
Đáp án D