Đồng phân là các hợp chất có cùng công thức phân tử nhưng có cấu trúc phân tử khác nhau. Trong trường hợp này, chúng ta đang xét đến đồng phân của C6H14. Đồng phân này có thể có nhiều cách đặt các nguyên tử hiđrocacbon trong phân tử, tạo ra các cấu trúc cấu tạo khác nhau.
CÔNG TY LUẬT TNHH DƯƠNG GIA
TRỤ SỞ CHÍNH TẠI HÀ NỘI
Địa chỉ: Số 89 Tô Vĩnh Diện, phường Khương Đình, thành phố Hà Nội.
Tổng đài tư vấn pháp luật: 1900.6568
Số điện thoại Luật sư: 037.6999996
Email: dichvu@luatduonggia.vn
Mục lục bài viết
1. Đồng phân của C6H14 và gọi tên, công thức cấu tạo C6H14:
C6H14 đồng phân cấu tạo:
Độ bất bão hòa k = số liên kết π + số vòng = (6.2 + 2 – 14) / 2 = 0
Phân tử không có chứa liên kết π hoặc 1 vòng ⇒ Phân tử chỉ chứa liên kết đơn
Hexan C6H14 có5 đồng phân mạch cacbon:
Viết các đồng phân cấu tạo của C6H14và gọi tên
CH3-CH2-CH2-CH2-CH2-CH3
n-hexan
CH3-CH(CH3)-CH2-CH2-CH3
2-metylpentan
CH3-CH2-CH(CH3)-CH2-CH3
3-metylpentan
(CH3)2-CH-CH(CH3)2
2,2 – đimetylbutan
(CH3)3-C-CH2-CH3
2,3- đimetybutan
Vậy C6H14 có 5 đồng phân cấu tạo.
Công thức cấu tạo:
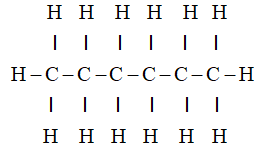
Cách tính số đồng phân Ankan CnH2n+2 (n ≥ 1).
Khái niệm: Ankan là những hiđrocacbon no, mạch hở, tức là chỉ chứa các liên kết đơn giữa các nguyên tử cacbon và hydro.
CTTQ: CnH2n+2(n ≥ 1).
Ankan là một nhóm các hợp chất hữu cơ quan trọng, có công thức chung là CnH2n+2. Đây là dạng đơn giản nhất của các hidrocarbon no, chỉ chứa liên kết đơn giữa các nguyên tử cacbon và hydro.
Để tính toán số đồng phân của Ankan, chúng ta cần xem xét số lượng và vị trí các nguyên tử cacbon trong phân tử. Khi số lượng nguyên tử cacbon lớn hơn hoặc bằng 4, chúng ta có thể tạo ra các đồng phân mạch C bằng cách thay đổi cấu trúc mạch cacbon.
Ví dụ, khi có phân tử C4H10 trở đi, ta thấy rằng mỗi công thức phân tử tương ứng có thể có các cấu trúc mạch cacbon không phân nhánh và mạch cacbon phân nhánh, tạo nên các đồng phân mạch cacbon khác nhau. Điều này cho phép chúng ta có nhiều sự đa dạng trong cấu trúc và tính chất của các đồng phân Ankan.
Vì vậy, để tính toán số đồng phân của Ankan, chúng ta cần xác định số lượng và vị trí các nguyên tử cacbon trong phân tử, sau đó tạo ra các đồng phân mạch C bằng cách thay đổi cấu trúc mạch cacbon. Qua đó, chúng ta có thể khám phá và hiểu rõ hơn về tính chất và ứng dụng của các hợp chất Ankan.
Công thức tính nhanh 2n – 4 + 1 (3 < n < 7)
2. Tính chất vật lý và tính chất hóa học:
Tính chất vật lí
Ở điều kiện bình thường, hexan tồn tại ở trạng thái lỏng trong suốt và được sử dụng như một dung môi không phân cực. Hexan có một mùi đặc trưng và được biết đến với độc tính thấp, làm cho nó an toàn khi sử dụng trong nhiều ứng dụng khác nhau. Đặc biệt, hexan được sử dụng rộng rãi trong lĩnh vực hóa học và công nghiệp để làm dung môi cho các phản ứng hóa học và quá trình sản xuất. Với tính chất không phân cực, hexan cũng được sử dụng trong phân tích và kiểm tra các chất không phân cực khác.
Tuy nhiên, như với bất kỳ chất liệu hóa học nào, cần thận trọng khi sử dụng hexan và tuân thủ các quy tắc an toàn để tránh nguy cơ tiềm ẩn. Cần đảm bảo rằng hexan được lưu trữ và vận chuyển đúng cách, tránh tiếp xúc với nguồn nhiệt và lửa, và hạn chế tiếp xúc trực tiếp với da và mắt. Ngoài ra, việc sử dụng thiết bị bảo hộ như găng tay, mắt kính và áo choàng bảo hộ là rất quan trọng khi làm việc với hexan.
Ngoài những điều trên, cần nhớ rằng hexan cũng có thể gây cháy và gây ngộ độc nếu hít phải hoặc nuốt phải lượng lớn. Vì vậy, cần thực hiện các biện pháp bảo vệ cá nhân và tuân thủ quy tắc an toàn trong quá trình sử dụng hexan. Điều này bao gồm việc làm việc trong một môi trường thoáng khí, sử dụng hệ thống thông gió hiệu quả và đảm bảo sự thoát khí an toàn khi làm việc với hexan.
Việc xử lý hexan cũng đòi hỏi sự chú ý đặc biệt. Cần tránh tiếp xúc với nhiệt độ cao và nguồn nhiệt mạnh, vì hexan có thể cháy và gây nguy hiểm. Đồng thời, cần lưu ý về việc xử lý chất thải hexan. Chất thải hexan phải được xử lý theo quy định và quy trình phù hợp để đảm bảo không gây ô nhiễm môi trường và nguy hiểm cho con người.
Nếu xảy ra sự cố hoặc nghi ngờ về việc tiếp xúc với hexan, cần ngay lập tức sử dụng biện pháp cấp cứu và tìm kiếm sự giúp đỡ y tế. Cần luôn nhớ rằng đối với các chất hóa học như hexan, sự an toàn và tuân thủ quy tắc an toàn là rất quan trọng để bảo vệ sức khỏe và sự phát triển đối với sức khỏe của mọi người xung quanh.
Tính chất hóa học
Ở điều kiện bình thường, hexan tồn tại ở trạng thái lỏng trong suốt và được sử dụng như một dung môi không phân cực. Hexan có một mùi đặc trưng và được biết đến với độc tính thấp, làm cho nó an toàn khi sử dụng trong nhiều ứng dụng khác nhau. Đặc biệt, hexan được sử dụng rộng rãi trong lĩnh vực hóa học và công nghiệp để làm dung môi cho các phản ứng hóa học và quá trình sản xuất. Với tính chất không phân cực, hexan cũng được sử dụng trong phân tích và kiểm tra các chất không phân cực khác.
Tuy nhiên, như với bất kỳ chất liệu hóa học nào, cần thận trọng khi sử dụng hexan và tuân thủ các quy tắc an toàn để tránh nguy cơ tiềm ẩn. Cần đảm bảo rằng hexan được lưu trữ và vận chuyển đúng cách, tránh tiếp xúc với nguồn nhiệt và lửa, và hạn chế tiếp xúc trực tiếp với da và mắt. Ngoài ra, việc sử dụng thiết bị bảo hộ như găng tay, mắt kính và áo choàng bảo hộ là rất quan trọng khi làm việc với hexan.
Hexan cũng có thể gây cháy và gây ngộ độc nếu hít phải hoặc nuốt phải lượng lớn. Nếu xảy ra sự cố hoặc nghi ngờ về việc tiếp xúc với hexan, cần ngay lập tức sử dụng biện pháp cấp cứu và tìm kiếm sự giúp đỡ y tế.
Phản ứng tách (gãy liên kết )
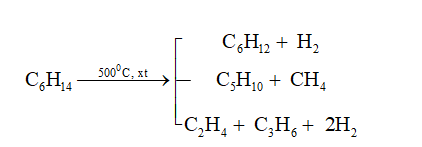
Dưới tác dụng của nhiệt và xúc tác như Cr2O3, Fe, Pt,…, các hợp chất hidrocacbon không chỉ bị phân hủy thành các hidrocacbon không no mà còn bị phá vỡ các liên kết C-C, từ đó tạo ra các phân tử nhỏ hơn. Quá trình này diễn ra do tác động của nhiệt độ và sự hiện diện của các chất xúc tác như Cr2O3, Fe, Pt,… Các hidrocarbon có thể bị tách thành các phân tử nhỏ hơn thông qua quá trình phân hủy, và các liên kết C-C trong chúng bị phá vỡ. Điều này xảy ra dưới tác dụng của nhiệt và xúc tác như Cr2O3, Fe, Pt,…
Phản ứng oxi hóa
Khi đốt, pentan bị cháy tạo ra CO2, H2O và tỏa nhiều nhiệt. Quá trình cháy của pentan là một quá trình oxi hóa hoàn toàn, trong đó pentan phản ứng với oxi trong không khí để tạo ra các sản phẩm cháy chính là CO2 và H2O. Trong quá trình này, năng lượng được giải phóng dưới dạng nhiệt, tạo nên hiện tượng tỏa nhiệt. Đây là một quá trình tự nhiên và phổ biến trong các quá trình đốt cháy của các chất hữu cơ.
Nếu không đủ oxi, quá trình đốt cháy pentan sẽ không hoàn toàn, dẫn đến việc tạo ra các sản phẩm như CO, than muội và các chất gây ô nhiễm khác, ngoài ra còn có CO2 và H2O. Tuy các sản phẩm này giúp giảm năng suất tỏa nhiệt, nhưng đồng thời cũng gây hại cho môi trường. Do đó, việc đảm bảo đủ lượng oxi trong quá trình đốt cháy pentan là rất quan trọng để đảm bảo hiệu suất và bảo vệ môi trường.
3. Điều chế:
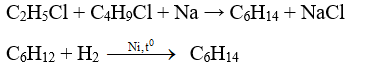
4. Các ứng dụng của HEXAN:
Lợi ích
HEXAN là một chất hóa học được sản xuất từ dầu thô và được sử dụng rộng rãi như là một dung môi để chiết xuất các loại dầu thực vật, bao gồm dầu đậu nành, dầu đậu phộng và dầu hướng dương. Điều này giúp tối ưu hóa quá trình sản xuất và cung cấp các sản phẩm tự nhiên.
Ngoài ra, HEXAN còn được ứng dụng trong nhiều lĩnh vực khác, bao gồm ngành dệt, trang trí nội thất, sản xuất giày, công nghệ in, mực in, sơn phủ, keo dán và băng dính. Sự đa dạng trong việc sử dụng chất này cho thấy tính linh hoạt và đa năng của HEXAN.
Đồng thời, HEXAN cũng được sử dụng làm dung môi tẩy rửa và dầu mỡ. Điều này giúp tăng cường khả năng làm sạch và bảo dưỡng các bề mặt và máy móc.
Tác hại
Tuy nhiên, cần lưu ý rằng HEXAN cũng có những tác hại đối với môi trường và sức khỏe con người. Theo Trung tâm Phòng chống Dịch bệnh Hoa Kỳ, HEXAN là một chất gây ô nhiễm môi trường và có thể gây hại đến hệ thần kinh.
Vì vậy, khi sử dụng HEXAN, cần tuân thủ các biện pháp an toàn và bảo vệ môi trường để giảm thiểu tác động tiêu cực.




