Mục lục bài viết
1. Cho viên Na vào dung dịch CuSO4, hiện tượng quan sát được là:
A. Bọt khí.
B. Bọt khí và kết tủa màu xanh.
C. Kết tủa màu đỏ.
D. Bọt khí và kết tủa màu đỏ.
Đáp án B
Phương trình: 2Na + 2H2O → 2NaOH + H2↑
2NaOH + CuSO4 → Cu(OH)2 ↓ + Na2SO4
2. Cho một mẩu Na vào dung dịch CuSO4, hiện tượng xảy ra là:
A. có khí thoát ra, xuất hiện kết tủa xanh, sau đó kết tủa tan
B. dung dịch mất màu xanh, xuất hiện Cu màu đỏ
C. có khí thoát ra, xuất hiện kết tủa xanh, kết tủa không tan
D. dung dịch có màu xanh, xuất hiện Cu màu đỏ.
Na sẽ tác dụng với nước trong dung dịch trước:
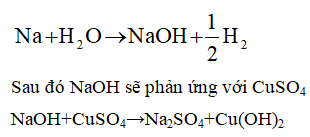
3. Bài tập vận dụng có lời giải:
Bài tập 1: Hòa tan 58g muối CuSO4.5H2O vào nước được 500ml dung dịch A. Cho dần dần bột sắt vào 50ml dung dịch A, khuẩy nhẹ cho tới khi dung dịch hết màu xanh. Tính lượng sắt đã tham gia phản ứng.
Lời giải:
Fe + CuSO4 → FeSO4 + Cu.
nFe = nCuSO4 = 0,232 mol.
mFe = 0,232 x 56 = 12,992g.
Bài tập 2: Hòa tan 12,5 gam tinh thể CuSO4.5H2O trong nước thành 200 ml dung dịch . Tính nồng độ mol các ion trong dung dịch thu được .
0,05 0,05 0,05 (mol)
[ Cu2+] = [SO42-] = 0,05/0,2 = 0,25 (M)
Bài tập 3: Hoà tan 25 gam muối CuSO4.5H2O vào nước được 500 ml dung dịch. Cho dần mạt sắt vào 50 ml dung dịch trên, khuấy nhẹ cho đến khi hết màu xanh. Khối lượng chất rắn thu được sau phản ứng tăng hay giảm bao nhiêu gam ?
Lời giải:
Tăng 0.08 gam
Bài tập 4: Hòa tan 50 gam tinh thể CuSO4.5H2O vào 200 ml dung dịch HCl 0,6 M thu được dung dịch X. Đem điện phân dung dịch X (các điện cực trơ) với cường độ dòng điện 1,34A trong 4 giờ. Khối lượng kim loại thoát ra ở catot và thể tích khí thoát ra ở anot (ở đktc) lần lượt là (Biết hiệu suất điện phân là 100 %)
Lời giải:
6.4 gam và 1.792 lít
Bài tập 5: Hoà tan 100g cuso4.5h2o vào 400gam dung dịch cuso4 4%. Tìm nồng độ phần trăm của dung dịch thu đc
Lời giải:
nCuSO4.5H2O=100/250 = 0,4(mol)
=> nCuSO4(tinh thể)=0,4(mol)
mCuSO4(ban đầu)= 16(g)
=> Tổng mCuSO4= 80(g)
mddCuSO4= 100+400=500(g)
=> C% dd CuSO4 = (80/500)*100%= 16%
Bài tập 6: Cần lấy bao nhiêu gam tinh thể CuSO4.5H2O và bao nhiêu gam dung dịch CuSO4 4% để điều chế 500 gam dung dịch CuSO4 8%?
Gợi ý giải:
Gọi mCuSO4.5H2O = x gam; mCuSO4 4% = y gam.
Lập hệ PT để tìm x và y dựa vào:
+ Khối lượng dung dịch CuSO4 8%.
+ Lượng chất tan có trong dung dịch CuSO4 8%.
Bài tập 7: Nêu phương trình
- đồng 2 sunfat tác dụng với sắt
- đồng sunfat tác dụng với natri hidroxit
Gợi ý giải:
Fe + CuSO4 → FeSO4 + Cu↓
CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
Bài 8. Ngâm một chiếc đinh sắt vào dung dịch CuCl2. Hiện tượng nào sau đây là đúng?
A. Có chất rắn màu đỏ bám ngoài đinh sắt, màu xanh dung dịch nhạt dần.
B. Có chất rắn màu đỏ bám ngoài đinh sắt, dung dịch chuyển sang màu vàng nâu.
C. Xuất hiện bọt khí không màu bay lên.
D. Không có hiện tượng gì.
Câu 9. Nhỏ từ từ dung dịch NaOH vào dung dịch CuCl2 đển khi kết tủa không tạo thêm nữa thì dừng lại. Lọc kết tủa rồi đem nung đến khối lượng không đổi. Thu được chất rắn nào sau đây:
A. Cu
B. CuO
C. Cu2O
D. Cu(OH)2
Câu 10. Trường hợp nào sau đây có phản ứng tạo sản phẩm là chất kết tủa màu xanh?
A. Cho dung dịch NaOH vào dung dịch CuSO4
B. Cho Zn vào dung dịch AgNO3
C. Cho Al vào dung dịch HCl
D. Cho dung dịch KOH vào dung dịch FeCl3
Câu 11. Thí nghiệm tạo ra muối sắt (III) sunfat là
A. sắt phản ứng với dung dịch H2SO4 đặc nóng.
B. sắt phản ứng với dung dịch H2SO4 loãng.
C. sắt phản ứng với dung dịch CuSO4.
D. sắt phản ứng với dung dịch Al2(SO4)3.
Câu 12. Ngâm một cây đinh sắt sạch vào dung dịch bạc nitrat. Hiện tượng xảy ra là
A. sắt bị hòa tan một phần, bạc được giải phóng.
B. bạc được giải phóng nhưng sắt không biến đổi.
C. không có chất nào sinh ra, chỉ có sắt bị hòa tan.
D. không xảy ra hiện tượng gì.
Câu 13. Nhúng một thanh sắt vào dung dịch CuSO4, sau một thời gian thấy khối lượng chất rắn tăng 1,6 gam. Số mol CuSO4 đã tham gia phản ứng là:
A. 0,1 mol.
B. 0,2 mol.
C. 0,3 mol.
D. 0,4 mol.
Câu 14. Tiến hành thí nghiệm bỏ vào dung dịch HCl vừa đủ kim loại Fe và Cu. Các chất thu được sau phản ứng là
A. FeCl2 và H2.
B. FeCl2, Cu và H2.
C. Cu và khí H2.
D. FeCl2 và Cu.
Câu 15. Cho 5,6 gam bột Fe vào dung dịch CuSO4 dư, sau phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 3,2.
B. 6,5.
C. 6,4.
D. 12,9.
Câu 16. Cho hỗn hợp kim loại X gồm: Cu, Fe, Mg. Lấy 10,88 gam X tác dụng với clo dư thu được 28,275 gam chất rắn. Nếu lấy 0,44 mol X tác dụng với axit HCl dư thu được 5,376 lít khí H2 (đktc). Giá trị thành phần % về khối lượng của Fe trong hỗn hợp X gần với giá trị nào sau đây nhất ?
A. 58,82%
B. 25,73%
C. 22,69%
D. 22,69%
Câu 17: Trình bày về các phương pháp tổng hợp đồng sunphat từ nguyên liệu đơn giản, ví dụ như từ đồng kim loại
Lời giải chi tiết:
Có một số phương pháp tổng hợp đồng sunphat từ nguyên liệu đơn giản như đồng kim loại. Dưới đây là hai phương pháp phổ biến:
Phản ứng trực tiếp giữa đồng kim loại và axit sunfuric:
Phương trình hóa học: Cu + H2SO4 → CuSO4 + H2
Giải thích: Phương pháp này liên quan đến việc đồng kim loại (ví dụ như lá đồng) phản ứng trực tiếp với axit sunfuric để tạo ra đồng sunphat. Trong quá trình này, đồng reagiert với axit sunfuric tạo thành dung dịch đồng sunphat và khí hydro. Quá trình này thường được thực hiện dưới điều kiện nhiệt độ và áp suất cụ thể để tạo ra sản phẩm với hiệu suất cao hơn.
Quá trình oxi hóa của đồng kim loại:
Phương trình hóa học: 4Cu + O2 + 2H2SO4 → 2CuSO4 + 2H2O
Giải thích: Đây là quá trình oxit hóa của đồng kim loại (đồng trong dạng tinh khiết hoặc hợp kim) trong môi trường axit sunfuric với sự có mặt của không khí. Trong quá trình này, đồng được oxit hóa thành đồng sunphat và nước. Phương pháp này thường được sử dụng trong quá trình công nghiệp để sản xuất lớn lượng đồng sunphat từ nguyên liệu đồng tinh khiết hoặc từ quá trình tái chế đồng từ các loại nguyên liệu có chứa đồng.
Cả hai phương pháp này đều tạo ra đồng sunphat từ đồng kim loại thông qua phản ứng với axit sunfuric, và chúng có thể được điều chỉnh về điều kiện và quy trình để đảm bảo hiệu suất sản xuất cao nhất.
Bài 18: Diễn đạt về các quá trình sản xuất đồng sunphat trong ngành công nghiệp và các phương pháp tinh lọc và chiết tách.
Lời giải chi tiết:
Quá trình sản xuất đồng sunphat trong ngành công nghiệp thường bắt đầu từ nguyên liệu đồng tinh khiết hoặc từ các nguồn đồng chứa trong quặng.
– Phương pháp điện phân:
Trong phương pháp này, quặng đồng được nghiền và xay nhỏ, sau đó hòa tan trong axit sunfuric để tạo ra dung dịch đồng sunphat.
Dung dịch đồng sunphat sau đó được đưa vào hệ thống điện phân, trong đó điện phân dung dịch này để tạo ra đồng sunphat rắn ở cực âm (cathode).
Đồng sunphat được tách ra từ dung dịch, rửa sạch và sau đó được chế biến thành các sản phẩm cuối cùng, như hóa chất, phân bón hoặc sử dụng trong ngành công nghiệp khác.
– Phương pháp hoá học:
Quặng đồng được xử lý bằng axit sunfuric để hòa tan đồng và tạo ra dung dịch đồng sunphat.
Dung dịch này sau đó được xử lý với các phương pháp chiết tách hoặc kết tủa để tách đồng sunphat ra khỏi dung dịch.
Đồng sunphat rắn sau đó được tinh lọc, lọc bỏ các tạp chất và được tiếp tục xử lý để sản xuất các sản phẩm cuối cùng.
– Phương pháp tinh lọc và chiết tách:
+ Chiết tách:
Trong các bước sản xuất và xử lý, các phương pháp chiết tách có thể được sử dụng để tách riêng các thành phần khác nhau trong dung dịch hoặc hỗn hợp.
Đối với sản xuất đồng sunphat, chiết tách có thể được sử dụng để tách đồng sunphat từ các chất cặn, chất tạp hoặc các kim loại khác có thể có trong dung dịch.
+ Tinh lọc:
Sau khi tạo ra đồng sunphat, quá trình tinh lọc là cần thiết để loại bỏ các tạp chất, các hạt không mong muốn, và các chất cặn khác trong sản phẩm.
Các phương pháp tinh lọc có thể bao gồm sử dụng các bộ lọc, quá trình lắng đọng, hay các phương pháp khác để tách riêng chất tinh khiết và loại bỏ các chất phụ trợ.
Cả hai phương pháp tinh lọc và chiết tách đều đóng vai trò quan trọng trong việc sản xuất đồng sunphat từ nguyên liệu đồng, giúp sản phẩm cuối cùng đạt được độ tinh khiết cao và đáp ứng được các tiêu chuẩn chất lượng.