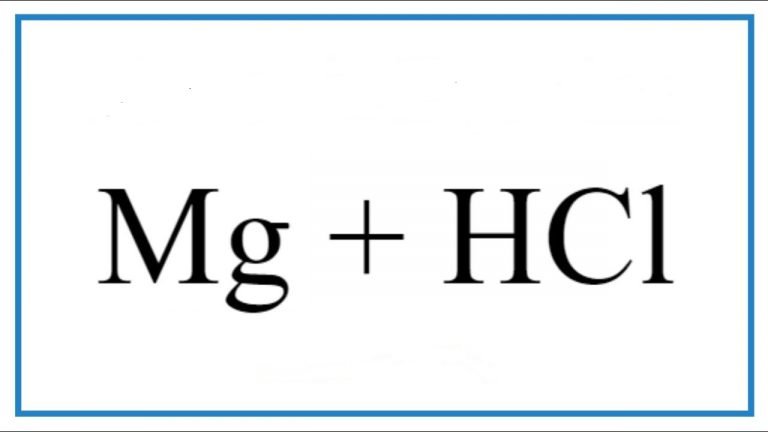Canxi phản ứng với nước để tạo ra hidroxit canxi và khí hydro, theo phương trình hóa học: Ca + H2O → Ca(OH)2 + H2. Sự phản ứng khí hydro trong phản ứng này cũng rất quan trọng vì nó có thể được sử dụng làm nguồn năng lượng cho các ứng dụng khác nhau, bao gồm động cơ xe và phát điện.
Mục lục bài viết
1. Phương trình phản ứng Ca tác dụng H2O:
Phản ứng giữa Canxi (Ca) và Nước (H2O) là một trong những phản ứng hóa học đơn giản nhất, nhưng lại rất quan trọng trong cuộc sống hàng ngày của chúng ta. Phản ứng này được biểu diễn bằng phương trình hóa học:
Ca + 2H2O → Ca(OH)2 + H2
Phương trình cho thấy rằng phản ứng giữa Canxi và Nước tạo ra Canxi Hydroxit (Ca(OH)2) và Khí Hiđro (H2). Canxi Hydroxit là một chất rắn, còn Khí Hiđro là một khí không màu, không mùi, không vị và không độc hại. Phản ứng này có thể được sử dụng trong nhiều lĩnh vực, chẳng hạn như trong sản xuất xi măng, thuốc trừ sâu, cũng như trong các ứng dụng công nghiệp khác.
2. Điều kiện phản ứng giữa kim loại Ca và H2O:
Phản ứng giữa Canxi và Nước là một phản ứng tự nhiên, không cần phải tạo ra bất kỳ điều kiện đặc biệt nào. Tuy nhiên, việc điều chỉnh một số yếu tố như nhiệt độ, áp suất, pH hoặc sử dụng các chất xúc tác có thể làm tăng tốc độ phản ứng. Khi nhiệt độ, áp suất hoặc pH được điều chỉnh thích hợp, phản ứng sẽ diễn ra nhanh hơn và hiệu quả hơn.
3. Cách thực hiện phản ứng kim loại Ca với H2O:
Để thực hiện phản ứng giữa Canxi và Nước, ta có thể làm như sau:
Chuẩn bị một mẫu Canxi (Ca)
Đưa mẫu Canxi vào cốc chứa Nước cất (H2O)
Khi đưa mẫu Canxi vào trong Nước, ta có thể quan sát được hiện tượng phản ứng xảy ra.
Thao tác trên nên được thực hiện cẩn thận để đảm bảo an toàn, bảo vệ sức khỏe và tránh gây hư hại cho môi trường.
4. Hiện tượng nhận biết phản ứng kim loại Ca với H2O:
Khi Canxi được đưa vào Nước, chất rắn Canxi (Ca) sẽ dần tan dần trong Nước và tạo ra Khí Hiđro (H2) sủi bọt khí trong dung dịch. Việc phát hiện được Khí Hiđro này cũng là một cách nhận biết phản ứng giữa Canxi và Nước đã xảy ra. Ngoài ra, nếu ta sử dụng giấy pH để đo pH của dung dịch Nước và Canxi Hydroxit, ta cũng có thể quan sát được sự thay đổi pH của dung dịch và từ đó xác định được phản ứng đã diễn ra hoặc không. Việc hiểu rõ về các hiện tượng liên quan đến phản ứng giữa Canxi và Nước là rất quan trọng trong việc ứng dụng và phát triển công nghệ trong các lĩnh vực khác nhau.
5. Ca là gì?
Ca là ký hiệu hóa học của Canxi trong bảng tuần hoàn nguyên tố hóa học. Canxi là một nguyên tố vô cùng quan trọng đối với sự tồn tại của con người và các loài sinh vật khác. Nó là một kim loại kiềm thổ, có màu trắng bạc, dẻo và khá cứng. Canxi là thành phần chính của xương và răng, giúp chúng ta duy trì sự vững chắc và độ cứng của chúng. Ngoài ra, nó còn giúp cơ thể chúng ta hoạt động bình thường, như truyền dẫn xung thần kinh, co bóp cơ và ức chế sự co bóp của cơ.
Nếu không đủ canxi, cơ thể sẽ bắt đầu rút canxi từ xương và răng, dẫn đến các vấn đề về xương và răng, chẳng hạn như loãng xương và răng sâu. Vì vậy, việc bổ sung canxi vào chế độ ăn uống là vô cùng quan trọng.
Canxi cũng có nhiều đồng vị khác nhau, trong đó 2 đồng vị tự nhiên được tìm thấy trong tự nhiên là Ca40 và Ca41, với chu kỳ bán rã là 103.000 năm. Còn lại là đồng vị được tạo ra trong phòng thí nghiệm. Tuy nhiên, khoảng 97% của canxi tồn tại dưới dạng Ca40.
Ngoài ra, canxi cũng có thể bị phủ màng oxit-hiđroxit khi tiếp xúc với không khí ẩm, điều này có thể làm giảm tính chất của nó. Tóm lại, canxi là một nguyên tố quan trọng đối với sức khỏe và sự phát triển của con người và các loài sinh vật khác. Việc bổ sung canxi đúng cách là vô cùng cần thiết để duy trì sức khỏe và sự phát triển của chúng ta.
5.1. Tính chất hóa học của Ca (Canxi):
Oxit bazơ của canxi, còn được gọi là vôi quicklime, là một hợp chất vô cơ có công thức hóa học CaO. Được sản xuất thông qua quá trình nung đốt đá vôi tại nhiệt độ cao, canxi oxit là một chất rắn màu trắng, mịn và có tính ăn mòn cao.
Tuy nhiên, canxi oxit cũng có nhiều ứng dụng rộng rãi trong đời sống. Trong ngành xây dựng, vôi quicklime được sử dụng để sản xuất xi măng, một loại vật liệu xây dựng quan trọng. Canxi oxit cũng được sử dụng trong sản xuất sơn, giúp tăng độ bền và độ bóng của bề mặt sơn.
Ngoài ra, canxi oxit còn được sử dụng như một chất xúc tác trong các quá trình hóa học và trong sản xuất thuốc trừ sâu.
Canxi oxit cũng có khả năng tác dụng với nước, tạo ra Ca(OH)2, một hợp chất ít tan trong nước. Phản ứng này được gọi là phản ứng tôi vôi và có khả năng tỏa nhiều nhiệt.
Ngoài ra, canxi oxit còn có khả năng tác dụng với axit, tạo ra các sản phẩm như CaCl2 và H2O, CaSO4 và H2O, hoặc Ca(NO3)2 và H2O. Canxi oxit cũng có thể tác dụng với oxit axit tạo ra các sản phẩm như CaCO3, CaSO3 và Ca3(PO4)2.
Tóm lại, canxi oxit là một hợp chất vô cùng quan trọng và được sử dụng rộng rãi trong đời sống.
5.2. Ứng dụng của Canxi:
Canxi là một thành phần cần thiết cho sức khỏe của con người, đặc biệt là sự hình thành và tăng trưởng của xương và răng. Tuy nhiên, không chỉ thiếu canxi mà thừa canxi cũng có thể gây ra những vấn đề về sức khỏe, chẳng hạn như sỏi thận. Để hấp thụ canxi, vitamin D cũng rất quan trọng. Bên cạnh việc sử dụng sữa và các sản phẩm chứa canxi để bổ sung cho cơ thể, canxi còn có nhiều ứng dụng khác trong cuộc sống. Ví dụ, canxi có thể được sử dụng như một chất khử trong việc điều chế các kim loại khác như uran, ziriconi hay thori. Ngoài ra, canxi cũng là một chất chống ôxi hóa, chống sulfua hóa hay chống cacbua hóa cho những loại kim loại tổng hợp chứa hay không chứa sắt. Canxi còn được sử dụng trong sản xuất xi măng hay vữa xây dựng, giúp cải thiện chất lượng và độ bền của các vật liệu xây dựng. Tóm lại, canxi không chỉ là một thành phần cần thiết cho sức khỏe mà còn có nhiều ứng dụng khác trong cuộc sống hàng ngày của chúng ta.
6. Bài tập vận dụng liên quan:
Câu 1. Vôi sống sau khi sản xuất phải được bảo quản trong bao kín. Nếu để lâu ngày trong không khí, vôi sống sẽ “chết”. Hiện tượng này được giải thích bằng phản ứng nào dưới đây?
A. Ca(OH)2 + CO2 → CaCO3 + H2O
B. CaO + CO2 → CaCO3
C. CaCO3 + CO2 + H2O → Ca(HCO3)2
D. CaO + H2O → Ca(OH)2
Đáp án B
Câu 2. Điện phân nóng chảy chất nào sau đây để điều chế kim loại canxi?
A. CaCO3.
B. Ca(NO3)2.
C. CaCl2.
D. CaSO4.
Đáp án C
Cau 3. Dãy kim loại tan hoàn toàn trong H2O ở điều kiện thường là:
A. Fe, Na, K.
B. Ca, Ba, K.
C. Ca, Mg, Na.
D. Al, Ba, K.
Đáp án B
Câu 4. Khi cho kim loại Ca vào các chất dưới đây, trường hợp nào không có phản ứng của Ca với nước?
A. dung dịch CuSO4 vừa đủ.
B. dung dịch HCl vừa đủ.
C. dung dịch NaOH vừa đủ.
D. H2O.
Đáp án B
Câu 5 : Cho dãy các kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là:
A. 2 B. 4 C. 3 D. 1
Đáp án C
Hướng dẫn giải:
Cu không tác dụng với H2O trong khi Fe tác dụng với nước ở nhiệt độ cao tạo thành các oxit sắt tương ứng. Tuy nhiên, giữa các kim loại khác trong bảng tuần hoàn cũng có những sự khác biệt về tính chất hóa học khi tương tác với nước. Chẳng hạn, kim loại Mg có thể tạo ra dung dịch bazơ nhẹ khi tác dụng với nước trong điều kiện thích hợp.
Vậy có 3 kim loại Na, Ca và K trong dãy tác dụng với nước ở nhiệt độ thường tạo dung dịch bazơ lần lượt là NaOH, Ca(OH)2 và KOH. Tuy nhiên, điều này không có nghĩa là các kim loại khác trong bảng tuần hoàn không tác dụng với nước để tạo ra dung dịch bazơ. Ví dụ, kim loại Ba cũng có khả năng tương tác với nước để tạo ra Ba(OH)2, một dung dịch bazơ mạnh hơn cả Ca(OH)2. Do đó, các tính chất hóa học của các kim loại trong bảng tuần hoàn là rất đa dạng và phong phú.
Câu 6: Khi cho kim loại Ca vào các chất dưới đây, trường hợp nào không có phản ứng của Ca với nước ?
A. dung dịch CuSO4 vừa đủ. B. dung dịch HCl vừa đủ.
C. dung dịch NaOH vừa đủ. D. H2O.
Đáp án B
Hướng dẫn giải:
Khi cho canxi (Ca) vào dung dịch axit clohidric (HCl), phản ứng hóa học sẽ xảy ra giữa hai chất theo phương trình hóa học:
Ca + 2HCl → CaCl2 + H2 ↑
Trong phản ứng này, canxi sẽ phản ứng với axit clohidric để tạo thành muối canxi clorua (CaCl2) và khí hiđro (H2) thoát ra. Phản ứng này là một trong những phản ứng hóa học cơ bản và được thường xuyên sử dụng trong các thí nghiệm hóa học cơ bản.
Tuy nhiên, cần lưu ý rằng phản ứng chỉ xảy ra khi canxi được đưa vào dung dịch axit clohidric, chứ không phải khi canxi được đưa vào dung dịch nước của axit clohidric. Điều này có nghĩa là canxi không phản ứng với nước trong dung dịch axit clohidric. Thực tế, nước trong dung dịch HCl chỉ đóng vai trò nằm trong cấu trúc của axit clohidric và không có vai trò trong phản ứng giữa canxi và axit clohidric.
Với phản ứng này, bạn có thể thấy rằng canxi và axit clohidric phản ứng với nhau để tạo thành muối và khí hiđro. Phản ứng này có thể đóng vai trò quan trọng trong nhiều lĩnh vực khác nhau, từ hóa học đến y học và công nghệ. Hi vọng thông tin này sẽ giúp bạn hiểu rõ hơn về phản ứng giữa canxi và axit clohidric.
Câu 7: Điều nào sau đây không đúng với canxi ?
A. Nguyên tử Ca bị oxi hóa khi Ca tác dụng với H2O
B. Ion Ca2+ bị khử khi điện phân CaCl2 nóng chảy
C. Nguyên tử Ca bị khử khi Ca tác dụng với H2
D. Ion Ca2+ không bị oxi hóa hay bị khử khi Ca(OH)2 tác dụng với HCl
Đáp án C
Hướng dẫn giải:
Ta có phương trình hóa học sau: Ca + H2 → CaH2 (canxi hidrua). Điều đáng chú ý là phản ứng này là một phản ứng oxi-hoá khử. Trong đó, chất khử là canxi (Ca) bị oxi hóa, còn chất oxi hóa là hidro (H2) bị khử. Ngoài ra, phản ứng này có ứng dụng trong sản xuất khí Acetylen và trong các quá trình sản xuất kim loại. Việc hiểu rõ về cơ chế phản ứng này cũng giúp cho chúng ta có thể phát triển các ứng dụng mới của canxi hidrua trong tương lai.