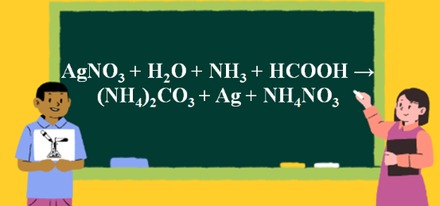Axit fomic tác dụng với AgNO3 trong dung dịch NH3 tạo ra kết tủa là Ag. Đây là phản ứng tráng gương, với mục đích là tạo kết tủa bạc sau khi kết thúc tiếp xúc. Axit fomic là chất lỏng, không màu và dễ bốc khói. Bài viết sau đây sẽ làm rõ phản ứng Axit fomic tác dụng với AgNO3 trong dung dịch NH3 và các khía cạch liên quan đến Axit fomic, mời các bạn cùng tham khảo!
Mục lục bài viết
1. Axit fomic tác dụng với AgNO3 trong NH3 tạo ra kết tủa:
Phương trình hóa học:
2 AgNO3 + H2O + 4 NH3 + HCOOH → (NH4)2CO3 + 2 Ag ↓ + 2 NH4NO3
Phản ứng giữa axit formic (HCOOH) và dung dịch AgNO3/ NH3 trong điều kiện tiêu biểu, phản ứng này không xảy ra, và điều này mang lại những thông tin quan trọng về tính chất hóa học của các chất tham gia.
– Tiến hành phản ứng: Bắt đầu bằng việc thêm axit formic vào dung dịch AgNO3 trong môi trường dung dịch NH3. Tại điều kiện này, các phức chất tạo thành từ ion Ag+ và NH3 có thể làm giảm khả năng tác động của axit formic, không tạo ra phản ứng hoặc tạo ra phản ứng có hiệu suất rất thấp.
– Hiện tượng: Phản ứng giữa axit formic (HCOOH) và dung dịch AgNO3 trong dung dịch NH3 tạo ra một hiện tượng hóa học đặc biệt và thú vị, được biết đến như phản ứng tráng gương. Trong quá trình này, axit formic tác động với ion bạc (Ag+) có mặt trong dung dịch AgNO3, tạo ra kết tủa trắng bạc (Ag). Ở đây, axit formic (HCOOH) tác động với ion bạc (Ag+) từ dung dịch AgNO3 trong môi trường dung dịch NH3. Quá trình này tạo ra kết tủa trắng bạc (Ag), đồng thời giải phóng khí nitơ (N2) và tạo thành nước (H2O) và CO2 (carbon dioxide) như sản phẩm phụ.
Axit fomic tác dụng với AgNO3 trong dung dịch NH3 tạo ra kết tủa là Ag. Đây là phản ứng tráng gương, với mục đích là tạo kết tủa bạc sau khi kết thúc tiếp xúc. Sự xuất hiện của kết tủa trắng bạc có thể được quan sát trực tiếp và thường được mô tả như là một lớp mỏng bạc phản ánh ánh sáng, tạo nên hiệu ứng tráng gương đặc trưng. Điều này là kết quả của sự kết tụ của các phân tử bạc (Ag) thành dạng kết tủa khi tương tác với axit formic.
2. Tính chất, ứng dụng và điều chế Axit Fomic:
Axit fomic có thể tác dụng với:
– Dung dịch HCOOH làm quỳ tím chuyển thành màu đỏ nhạt.
– Tác dụng với kim loại mạnh
2Na + 2HCOOH → 2HCOONa + H2
– Tác dụng với oxit bazơ.
CuO + 2HCOOH → (HCOO)2Cu + H2O
– Tác dụng với bazơ.
NaOH + HCOOH → HCOONa + H2O
– Tác dụng với muối của axit yếu hơn.
NaHCO3 + HCOOH → HCOONa + CO2 + H2O
– Phản ứng este hóa.
HCOOH + CH3OH → HCOOCH3 + H2O (Đây là phản ứng thuận nghịch được xúc tác nhờ axit sunfuric đặc và nhiệt độ).
– Phản ứng tráng gương.
HCOOH + 2[Ag(NH3)2]OH → (NH4)2CO3 + 2Ag↓ + 2NH3↑ + H2
Ứng dụng
– Dùng làm chất khử trùng và chất diệt khuẩn có giá trị trong nhiều ứng dụng làm sạch trong công nghiệp hoặc cũng được sử dụng phổ biến tại cuộc sống thường ngày.
– Là chất trung gian để làm dung môi trong các chất tạo khối còn được gọi là methanoic acid.
– Giúp điều chỉnh giá trị pH. Đây là vai trò mà axit fomic dùng để điều chỉnh giá trị pH trong khử lưu huỳnh khí thải, đông máu mủ và nhiều ứng dụng quan trọng khác.
Bên cạnh đó, Axit fomic còn được dùng để giúp tổng hợp hoá học và mạ điện, khai thác dầu khí, chất điều vị thực phẩm…
– Trong quá trình sử dụng axit fomic, cần mang trang phục bảo hộ lao động, tránh dây hóa chất vào tay hoặc mắt vì nó sẽ gây ảnh hưởng xấu đến sức khỏe.
Điều chế Axit Fomic
– Trong phòng thí nghiệm: Axit fomic có thể được điều chế trong phòng thí nghiệm bằng 2 cách:
+ Nung nóng acid oxalic trong glyxerol khan, sau đó chiết ra bằng cách chưng hơi.
+ Thủy phân acid etyl isonitril với xúc tác là dung dịch axit clohidric.
C2H5NC + 2H2O → C2H5NH2 + HCOOH
– Trong công nghiệp: Axit fomic trong công nghiệp được điều chế bằng cách:
+ Cách 1: Có một lượng đáng kể axit fomic được tạo ra qua quá trình điều chế các chất khác, đặc biệt là acid acetic. Trong quá trình này, acid formic là một sản phẩm phụ.
+ Cách 2: Cho methanol phản ứng cacbon monoxit trong điều kiện có xúc tác là bazo mạnh để tạo ra metyl fomiat, một dẫn xuất của axít fomic. Sau đó, tiến hành thủy phân metyl formiat để tạo ra axit fomic
CH3OH + CO → HCOOCH3
HCOOCH3 + H2O → HCOOH + CH3OH
+ Cách 3: Cho metyl formiat phản ứng với amoniac để tạo ra formamid, sau đó dùng axit sunfuric để thủy phân nhằm để tạo ra axit formic
NH3 + HCOOCH3 → HCONH2 + CH3OH
HCONH2 + ½H2SO4 + H2O → HCOOH + ½(NH4)2SO4
3. Bài tập liên quan kèm đáp án:
Bài tập 1: Cho các chất sau gồm: saccarozo, ancol benzylic, toluen, axit metacrylic, anilin, etilen, fructozo, SO2, stiren, CO2, phenol (C6H5OH), ancol benzylic. Số chất có khả năng làm mất màu nước brom là:
A. 7
B. 5
C. 6
D. 4
Đáp án C
Các chất có khả năng làm mất màu dung dịch nước Br2 bao gồm: etilen (CH2=CH2), axit metacrylic (CH2=CH-COOH), anilin (C6H5NH2), stiren (C6H5CH=CH2), phenol (C6H5OH), SO2. Do đó, có tổng cộng 6 chất thỏa mãn điều kiện đề bài.
Bài tập 2: Trong số các chất sau đây, chất có trong phản ứng tráng gương (tạo kết tủa bạc)?
A. HCOOC2H5
B. CH3-O-CH3
C. CH2=CH2
D. C2H5OH
Đáp án A
Chất HCOOC2H5 có khả năng tham gia phản ứng tráng gương do có cấu trúc HCOOR dạng RO-CHO, trong đó nhóm –CHO có khả năng tạo kết tủa bạc:
RO−CHO + 2 AgNO3 + 3 NH3 + H2O → ROCOONH4 + 2 Ag↓ + 2NH4NO3.
Bài tập 3: Đáp án nào có thể làm khô khí NH3 cũng như hơi nước?
A. P2O5.
B. H2SO4 đặc.
C. CuO bột.
D. NaOH rắn.
Đáp án D
Chất làm khô là chất có khả năng hút ẩm mạnh. Chất làm khô không tác dụng, không hòa tan với khí (cả khi có nước). Trong quá trình làm khô khí, không có sự giải phóng nhiệt.
Bài tập 4: Chất nào được dùng để phân biệt axit fomic và axit axetat?
A. CO2
B. Quỳ tím
C. NaOH
D. Dung dịch AgNO3/NH3
Đáp án D
Để phân biệt giữa axit fomic và axit axetic, có thể sử dụng dung dịch AgNO3/ NH3 làm thuốc thử.
Do axit fomic (HCOOH) chứa nhóm –CHO, trong khi axit axetic (CH3COOH) không có nhóm này, ta có thể sử dụng dung dịch AgNO3/ NH3 làm chất phân biệt giữa chúng. Trong quá trình phản ứng của axit fomic với dung dịch AgNO3/ NH3, sẽ xuất hiện kết tủa bạc (Ag):
HCOOH + 2 AgNO3 + 4 NH3 + H2O ⇌ (NH4)2CO3 + 2 Ag↓ + 2 NH4NO3
Ngược lại, trong trường hợp axit axetic, không xuất hiện hiện tượng này. Do đó, việc sử dụng dung dịch AgNO3/ NH3 là một cách đơn giản và hiệu quả để phân biệt giữa axit fomic và axit axetic.
Bài tập 5:
Tính bazơ của NH3 có thể giải thích qua các điểm:
A. Trên nguyên tử N của NH3 còn một cặp electron tự do, là nguồn electron dư có khả năng nhận proton.
B. Phân tử NH3 có ba liên kết cộng hóa trị, trong đó có một liên kết đơn và hai liên kết đôi giữa N và H, làm cho phân tử có tính phân cực và khả năng tương tác với các ion hay phân tử khác.
C. NH3 tan được nhiều trong nước, cho phép nó tương tác và tạo các ion OH- khi phản ứng với nước.
D. NH3 tác dụng với nước, tạo thành NH4OH, nơi một phần của phân tử NH3 đóng vai trò như một cấu trúc tạo ra ion OH- trong dung dịch.
Đáp án A
Sự tính bazơ của NH3 xuất phát từ việc nguyên tử N trong phân tử này còn một cặp electron tự do, không tham gia vào quá trình liên kết hóa học.
THAM KHẢO THÊM: