Mục lục bài viết
1. C6H5ONa + HCl → C6H5OH + NaCl:
– Phương trình phản ứng: C6H5ONa + HCl → C6H5OH + NaCl
– Phản ứng này thuộc loại phản ứng trao đổi.
– Điều kiện phản ứng xảy ra C6H5ONa + HCl → C6H5OH + NaCl: Cho dung dịch HCl vào dung dịch C6H5ONa dung dịch bị vẩn đục.
– Hiện tượng phản ứng giữa C6H5ONa + HCl → C6H5OH + NaCl: Cho dung dịch HCl vào ống nghiệm chứa 1 – 2 ml dung dịch C6H5ONa
2. Phương trình rút gọn của C6H5ONa + HCl → C6H5OH + NaCl:
C6H5O– + H+ → C6H5OH
Bước 1: Viết phương trình phân tử:
C6H5ONa + HCl → C6H5OH + NaCl
Bước 2: Viết phương trình ion đầy đủ bằng cách: chuyển các chất vừa dễ tan, vừa điện li mạnh thành ion; các chất điện li yếu, chất kết tủa, chất khí để nguyên dưới dạng phân tử:
C6H5O– + Na+ + H+ + Cl– → C6H5OH + Na+ + Cl–
Bước 3: Viết phương trình ion thu gọn từ phương trình ion đầy đủ bằng cách lược bỏ đi các ion giống nhau ở cả hai vế:
C6H5O– + H+ → C6H5OH
3. Bài tập vận dụng liên quan:
3.1. Mở rộng về phản ứng trao đổi trong dung dịch chất điện li:
Xét phản ứng:
Dung dịch A + dung dịch B → Sản phẩm.
– Phản ứng xảy ra trong dung dịch các chất điện li là phản ứng giữa các ion.
– Phản ứng trao đổi ion trong dung dịch các chất điện li chỉ xảy ra khi các ion kết hợp được với nhau tạo thành ít nhất 1 trong số các chất sau:
+ Chất kết tủa.
+ Chất điện li yếu.
+ Chất khí.
Thí dụ:
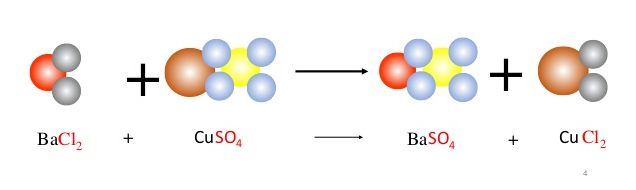
+ Phản ứng tạo thành chất kết tủa:
K2SO4 + BaCl2 → 2KCl + BaSO4↓
+ Phản ứng tạo thành chất điện li yếu:
HCl + KOH → KCl + H2O
+ Phản ứng tạo thành chất khí:
Zn + H2SO4 loãng → ZnSO4 + H2↑
3.2. Bài tập vận dụng liên quan:
Câu 1: Nhận xét nào sau đây đúng?
A. Phenol có tính axit mạnh hơn etanol
B. Phenol có tính axit yếu hơn etanol
C. Phenol dễ tan trong nước hơn trong dung dịch NaOH
D. Phenol không có tính axit.
Đáp án A
Loại C vì: Phenol ít tan trong nước
Loại D vì: Do ảnh hưởng của vòng benzen đến OH dẫn tới phenol có tính axit.
Loại B vì: Vòng benzen hút e của nhóm OH làm mật độ điện tích trên OH giảm, liên kết O-H phân cực mạnh hơn. Nguyên tử H của nhóm OH linh động hơn so với ancol nên phenol có tính axit mạnh hơn etanol
Câu 2: Hãy chọn phát biểu sai:
A. Phenol có tính axit yếu nhưng mạnh hơn H2CO3.
B. Phenol là chất rắn kết tinh dễ bị oxi hóa trong không khí.
C. Khác với benzen, phenol phản ứng dễ dàng với Br2 tạo kết tủa trắng.
D. Nhóm –OH và gốc phenyl ở phenol có ảnh hưởng qua lại lẫn nhau.
Đáp án A
Phenol có tính axit yếu hơn cả H2CO3.
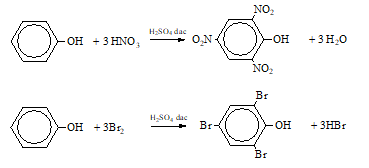
Câu 3:
Tên gọi của hợp chất Z là:
A.1,3,5-tribromphenol
B.2,4,6-tribromphenol
C.3,5-dibromphenol
D. phenolbromua
Đáp án B
Câu 4: Cho m gam hỗn hợp X gồm phenol và rượu etylic tác dụng với Na dư thu được 25,2 hỗn hợp muối. Cho m/10 gam lượng hỗn hợp X phản ứng vừa đủ với 10ml dung dịch NaOH 1M. Số mol của rượu và phenol là:
A. 0,1 và 0,1
B. 0,2 và 0,2
C. 0,2 và 0,1
D. 0,18 và 0,06
Đáp án C
C6H5OH + Na → C6H5ONa + 0,5 H2
x x mol
C2H5OH + Na → C2H5ONa + 0,5 H2
y y mol
C6H5OH + NaOH → C6H5ONa + H2O
0,01 0,01 mol
Câu 5: Một hỗn hợp phenol và rượu thơm X đơn chức. Lấy 20,2 gam hỗn hợp này tác dụng với Na dư thu được 2,24 lít khí H2 ở đktc. Mặt khác, cũng 20,2 gam hỗn hợp này phản ứng vừa đủ với 50 ml dung dịch NaOH 2M. Công thức phân tử của X là
A. C7H8O
B.C4H8O
C.C6H6O
D.C6H6O2
Đáp án A
Gọi công thức phân tử của X là ROH
Chỉ có phenol tác dụng với NaOH
C6H5OH + NaOH → C6H5ONa + H2O
0,1 0,1 mol
Có nX = nNaOH → MX =R + 17 =108. X là rượu thơm.
Công thức phân tử của X là C7H8O.
Câu 6: Vì sao phenol có lực axit mạnh hơn ancol và phản ứng thế vào nhân thơm ở phenol dễ hơn ở benzen ?
A. Do phenol có phân tử khối lớn hơn
B. Do ảnh hưởng qua lại giữa gốc phenyl và nhóm OH
C. Do liên kết hidro
D. Cả A và C
Đáp án B
Đó là do ảnh hưởng qua lại giữa gốc phenyl và nhóm hiđroxyl như sau:
Cặp electron chưa tham gia liên kết của nguyên tử oxi do ở cách các electron π của vòng benzen chỉ một liên kết α làm cho mật độ electron dịch chuyển vào vòng benzen. Điều đó dẫn tới các hệ quả sau:
* Liên kết O−H trở nên phân cực hơn, làm cho nguyên tử H linh động hơn. Tính axit mạnh hơn ancol.
* Mật độ electron ở vòng benzen tăng lên, nhất là ở các vị trí o và p, làm cho phản ứng thế dễ dàng hơn so với benzen và đồng đẳng của nó.
* Liên kết C−O trở nên bền vững so với ở ancol, vì thế nhóm OH phenol không bị thế bởi gốc axit như nhóm OH ancol.
Câu 7: Để sơ cứu cho người bị bỏng phenol người ta sử dụng hóa chất nào sau đây?
A. Glixerol
B. NaOH đậm đặc
C. H2SO4
D. NaCl
Đáp án A
Phenol tan nhiều trong glixerol nên glixerol sẽ kéo dần phenol ra ngoài.
NaOH đậm đặc phản ứng với phenol nhưng là hóa chất gây ăn mòn da, không được sử dụng để sơ cứu.
Câu 8: Cho các hợp chất thơm đều có CTPT C7H8O lần lượt tác dụng được với Na và NaOH thì số chất phản ứng được với Na, NaOH và không tác dụng được với cả Na và NaOH lần lượt là
A. 4, 3, 1
B. 4, 4, 0
C. 3, 3, 1.
D. 4, 3, 0
Đáp án A
Các hợp chất thơm có CTPT C7H8O là:
+ Phenol: o, m, p – CH3C6H4OH
+ Ancol: C6H5CH2OH
+ Ete: C6H5OCH3
– Tác dụng với Na: o, m, p – CH3C6H4OH; C6H5CH2OH (4 chất)
– Tác dụng với NaOH: o, m, p – CH3C6H4OH (3 chất)
– Không tác dụng với NaOH và Na: C6H5OCH3 (1 chất)
Câu 9: Cho phenol (C6H5OH) lần lượt tác dụng với (CH3CO)2O và các dung dịch NaOH; HCl; Br2; HNO3; CH3COOH. Số trường hợp xảy ra phản ứng là:
A. 4
B. 2
C. 1
D. 3
Đáp án A
Có 4 chất phản ứng với phenol là: (CH3CO)2O; NaOH; HNO3; Br2
PTHH:
(CH3CO)2O + C6H5OH → CH3COOC6H5 + CH3COOH (phản ứng điều chế este của phenol)
NaOH + C6H5OH → C6H5ONa + H2O
Câu 10: Phản ứng hóa học: C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3 (C6H5– là gốc phenyl) chứng tỏ:
A. Phenol có tính axit yếu hơn axit cacbonic
B. Phenol có tính axit mạnh hơn axit cacbonic
C. Phenol có tính oxi hóa mạnh hơn axit cacbonic
D. Phenol có tính oxi hóa yếu hơn axit cacbonic
Đáp án A
Phenol có tính axit yếu nó còn yếu hơn cả nấc 1 của axit H2CO3 và không làm đổi màu quỳ tím vì thế muối natriphenolat bị CO2 và H2O đẩy ra khỏi dd tạo thành phenol.
Câu 11: Cho sơ đồ chuyển hóa sau:
Các chất X, Y, Z lần lượt là
A. C6H5Br , C6H5OH , C6H5Cl
B. C6H5Br , C6H5ONa , C6H5OH
C. C6H5Br , C6H5ONa , C6H5Cl
D. C6H5Br , C6H5OH , HOC6H2(Cl)3.
Đáp án B
PTHH:
C6H6 + Br2 →Fe,to”>C6H5Br + HBr
C6H5Br + 2NaOH →to,p,xt”>C6H5ONa + H2O + NaBr
C6H5ONa + HCl → C6H5OH + NaCl
Cách cân bằng phương trình C6H5ONa + HCl → C6H5OH + NaCl:
Phương trình hóa học đã cho là:
C6H5ONa + HCl → C6H5OH + NaCl
Để cân bằng phương trình này, chúng ta cần đảm bảo số lượng nguyên tử của các nguyên tố trên cả hai phía của phương trình bằng nhau.
Ở phía trái:
C6H5ONa: có 1 nguyên tử carbon (C), 6 nguyên tử hydro (H), 1 nguyên tử oxi (O) và 1 nguyên tử natri (Na) HCl: có 1 nguyên tử hydro (H) và 1 nguyên tử clo (Cl)
Ở phía phải:
C6H5OH: có 1 nguyên tử carbon (C), 6 nguyên tử hydro (H) và 1 nguyên tử oxi (O) NaCl: có 1 nguyên tử natri (Na) và 1 nguyên tử clo (Cl)
Để cân bằng số lượng nguyên tử carbon (C), chúng ta cần thêm một phân tử C6H5ONa vào phía phải của phương trình:
C6H5ONa + HCl → C6H5OH + NaCl
Để cân bằng số lượng nguyên tử hydro (H), chúng ta cần thêm 6 phân tử HCl vào phía phải của phương trình:
C6H5ONa + 6HCl → C6H5OH + NaCl
Để cân bằng số lượng nguyên tử oxi (O), phương trình đã cân bằng.
Cuối cùng, để cân bằng số lượng nguyên tử natri (Na) và clo (Cl), chúng ta cần thêm 1 phân tử NaCl vào phía trái của phương trình:
C6H5ONa + 6HCl → C6H5OH + NaCl
Vậy phương trình đã được cân bằng.
Các mẹo để cân bằng phương trình hóa học chuẩn nhất C6H5ONa + HCl → C6H5OH + NaCl:
Để cân bằng phương trình hóa học C6H5ONa + HCl → C6H5OH + NaCl, bạn có thể làm theo các bước sau đây:
Bước 1: Xác định số nguyên tử các nguyên tố trong từng hợp chất:
C6H5ONa: Có 6 nguyên tử carbon (C), 6 nguyên tử hydro (H), 1 nguyên tử oxi (O) và 1 nguyên tử natri (Na). HCl: Có 1 nguyên tử hydro (H) và 1 nguyên tử clo (Cl). C6H5OH: Có 6 nguyên tử carbon (C), 6 nguyên tử hydro (H) và 1 nguyên tử oxi (O). NaCl: Có 1 nguyên tử natri (Na) và 1 nguyên tử clo (Cl).
Bước 2: So sánh số nguyên tử của mỗi nguyên tố giữa hai bên của phương trình hóa học và xác định xem phản ứng có cân bằng hay không.
Trên phía trái của phương trình: C: 6 nguyên tử (C6) trên cả hai hợp chất. H: 5 nguyên tử (H5) trong C6H5ONa, 1 nguyên tử (H1) trong HCl. O: 1 nguyên tử (O1) trong C6H5ONa. Na: 1 nguyên tử (Na1) trong C6H5ONa. Cl: 1 nguyên tử (Cl1) trong HCl.
Trên phía phải của phương trình: C: 6 nguyên tử (C6) trong C6H5OH. H: 6 nguyên tử (H6) trong C6H5OH. O: 1 nguyên tử (O1) trong C6H5OH. Na: 1 nguyên tử (Na1) trong NaCl. Cl: 1 nguyên tử (Cl1) trong NaCl.
Bước 3: Cân bằng số lượng các nguyên tử bằng cách thêm các hệ số phù hợp vào trước các chất.
C6H5ONa + HCl → C6H5OH + NaCl
C6H5ONa: 1 HCl: 1 C6H5OH: 1 NaCl: 1
Bước 4: Kiểm tra lại phương trình đã cân bằng.
C6H5ONa + HCl → C6H5OH + NaCl
C: 6 nguyên tử trên cả hai bên. H: 6 nguyên tử trên cả hai bên. O: 1 nguyên tử trên cả hai bên. Na: 1 nguyên tử trên cả hai bên. Cl: 1 nguyên tử trên cả hai bên.
Vậy, phương trình đã được cân bằng.