Mục lục bài viết
1. Phương trình phản ứng AgNO3 tác dụng NaCl:
AgNO3 + NaCl → AgCl↓ + NaNO3
Điều kiện phản ứng: Nhiệt độ thường
Hiện tượng phản ứng: Khi cho dung dịch AgNO3 tác dụng với dung dịch NaCl, sau phản ứng tạo thành bạc clorua không tan có màu trắng.
2. Phương trình rút gọn của AgNO3 + NaCl:
Phương trình phân từ: AgNO3 + NaCl → AgCl↓ + NaNO3
Phương trình ion:
Ag+ + NO3− + Na+ + Cl− → AgCl+ Na+ + NO3−
Phương trình ion thu gọn:
Ag+ + Cl− → AgCl ↓
3. Bài tập vận dụng liên quan:
Câu 1. Cho dung dịch AgNO3 vào dung dịch NaCl thì có hiện tượng là:
A. Có bọt khí thoát ra, dung dịch thu được không màu
B. Có xuất hiện kết tủa trắng
C. Dung dịch đổi màu vàng nâu
D. Không có hiện tượng gì xảy ra
Đáp án A
Câu 2. Cho dung dịch AgNO3 vào dung dịch NaCl thì có hiện tượng là:
A. Có bọt khí thoát ra, dung dịch thu được không màu
B. Có xuất hiện kết tủa trắng
C. Dung dịch đổi màu vàng nâu
D. Không có hiện tượng gì xảy ra
Đáp án B
Cho dung dịch AgNO3 vào dung dịch NaCl thì có hiện tượng là: Có xuất hiện kết tủa trắng
AgNO3 + NaCl → AgCl(↓ trắng) + NaNO3
Câu 3. Kết tủa hoàn toàn m gam NaCl bởi dung dịch AgNO3 dư thấy thu được 2,87 gam kết tủa. Giá trị của m là
A. 11,7 gam.
B. 1,71 gam.
C. 17,1 gam.
D. 1,17 gam.
Đáp án: Ý D
Câu hỏi. Kết tủa hoàn toàn m gam NaCl bởi dung dịch AgNO3 dư thấy thu được 2,87 gam kết tủa. Giá trị của m là
A. 11,7 gam.
B. 1,71 gam.
C. 17,1 gam.
D. 1,17 gam.
Đáp án D
nkết tủa = 2,87/143,5 = 0,02 mol
Phương trình phản ứng hóa học
AgNO3+ NaCl → AgCl↓ + NaNO3
0,02 ← 0,02
mNaCl = 0,2. 58,5 = 11,7 gam
Câu 3. Cho m gam muối NaCl tác dụng với dung dịch AgNO3 dư thì thu được một kết tủa , kết tủa này sau khi phản ứng phân hủy hoàn toàn cho 1,08 gam bạc. Tính giá trị của m
A. 0,585 gam
B. 5,850 gam
C. 1,17 gam
D. 1,755 gam
Câu 3. Cho m gam muối NaCl tác dụng với dung dịch AgNO3 dư thì thu được một kết tủa , kết tủa này sau khi phản ứng phân hủy hoàn toàn cho 1,08 gam bạc. Tính giá trị của m
A. 0,585 gam
B. 5,850 gam
C. 1,17 gam
D. 1,755 gam
Đáp án A
NaCl + AgNO3 → NaNO3 + AgCl
2AgCl 2Ag + Cl2
nAg =1,08/108=0,01 (mol)
==> nAgCl = nAg= 0,01 (mol)
nNaCl = nAgCl = 0,01 (mol)
==> mNaCl = 0,01.58,5=0,585 (g)
Vậy m = 0,585 gam.
Câu 4. Cho phản ứng NaOH + HCl → NaCl + H2O. Phản ứng hóa học nào sau đây có cùng phương trình ion thu gọn với phản ứng trên?
A. 2KOH + FeCl2 → Fe(OH)2 + 2KCl.
B. NaOH + NH4Cl → NaCl + NH3 + H2O.
C. NaOH + HNO3 → NaNO3 + H2O.
D. AgNO3 + NaCl → AgCl↓ + NaNO3
Đáp án C
Phương trình ion rút gọn của phản ứng NaOH + HCl → NaCl + H2O là:
OH– + H+ → H2O
A. 2OH– + Fe2+ → Fe(OH)2
B. OH– + NH4+ → NH3 + H2O
C. OH– + H+ → H2O
D. Ag+ + Cl– → AgCl
Câu 5. Trong các cặp chất cho dưới đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
A. AlCl3 và CuSO4.
B. NH3 và AgNO3.
C. AgNO3 và NaCl .
D. NaHSO4 và NaHCO3.
Đáp án A
Cặp chất có thể cùng tồn tại trong một dung dịch là không thể phản ứng với nhau
A đúng vì AlCl3 và CuSO4 không phản ứng với nhau
Loại B. NH3 và AgNO3.
2 AgNO3 + 2 NH3 + H2O → Ag2O + 2 NH4NO3
Loại C. AgNO3 và NaCl.
NaCl + AgNO3 → AgCl + NaNO3
D. NaHSO4 và NaHCO3.
NaHCO3 + NaHSO4 → Na2SO4 + CO2↑ + H2O
Câu 6. Cho một mẫu K vào 200ml dung dịch AlCl3 thu được 2,8 lit khí (đktc) và một kết tủa A. Nung A đến khối lượng không đổi thu được 2,55 gam chất rắn. Tính nồng độ mol/l của dung dịch AlCl3
A. 0,375M
B. 0,75M
C. 0,025M
D. 0,45M
Đáp án A
mrắn: Al2O3 → nAl2O3 = 0,025 mol
→ nAl(OH)3 = 0,05 mol
nKOH = 2nH2 = 0,25 mol.
TH1: KOH thiếu, chỉ có phản ứng.
3KOH + AlCl3 → Al(OH)3 + 3KCl
Không xảy ra vì số mol Al(OH)3 tạo ra trong phản ứng > số mol Al(OH)3 đề cho.
TH2: KOH dư, có 2 phản ứng xảy ra.
3KOH + AlCl3 → Al(OH)3+ 3KCl
0,15 → 0,05 → 0,05 mol
4KOH + AlCl3→ KAlO2 + 3KCl + H2O
(0,25 – 0,15) → 0,025
Tổng số mol AlCl3 phản ứng ở 2 phương trình là 0,075 mol
→ Nồng độ của AlCl3 = 0,375M
Câu 7. Cho m gam Fe tác dụng hết với dung dịch CuSO4 dư, thu được 28,8 gam Cu. Giá trị của m là
A. 50,4.
B. 12,6.
C. 16,8.
D. 25,2.
Đáp án D
nCu= 0,45 mol
Phương trình hóa học
CuSO4 + Fe → FeSO4+ Cu
0,45 ← 0,45 mol
⟹ mFe = 0,45.56 = 25,2 gam
Xem đáp án
Câu 8. Dung dịch ZnSO4 có lẫn tạp chất là CuSO4. Dùng kim loại nào sau đây để làm sạch dung dịch ZnSO4?
B. Zn
C. Cu
D. Mg
Đáp án A
Dùng kẽm vì có phản ứng:
Zn + CuSO4 → ZnSO4 + Cu ↓
Sau khi dùng dư Zn, Cu tạo thành không tan được tách ra khỏi dung dịch và thu được dung dịch ZnSO4 tinh khiết.
Không dùng Mg vì có phản ứng:
Mg + CuSO4 → MgSO4 + Cu ↓
Sau phản ứng có dd MgSO4tạo thành, như vậy không tách được dung dịch ZnSO4 tinh khiết.
Câu 9:
Có 3 lọ không nhãn, mỗi lọ đựng dung dịch muối sau: CuSO4, AgNO3, NaCl. Hãy dùng những dung dịch có sẵn trong phòng thí nghiệm để nhận biết chất đựng trong mỗi lọ. Viết các phương trình hóa học.
Lời giải:
Trích mẫu thử và đánh số thứ tự:
– Dùng dung dịch NaCl có sẵn trong phòng thí nghiệm lần lượt cho vào từng mẫu thử trên:
+ Có kết tủa trắng (AgCl) xuất hiện đó là mẫu thử AgNO3.
Phương trình hóa học:
NaCl + AgNO3 → AgCl↓ + NaNO3
+ Không có hiện tượng gì là CuSO4 và NaCl
– Dùng dung dịch NaOH có trong phòng thí nghiệm cho vào 2 mẫu còn lại:
+ Mẫu nào có kết tủa đó là sản phẩm của CuSO4.
Phương trình hóa học:
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4.
+ Không hiện tượng là NaCl.
Câu 10:
Hãy dẫn ra một dung dịch muối khi tác dụng với một dung dịch chất khác thì tạo ra:
a) chất khí.
b) chất kết tủa.
Viết các phương trình hóa học.
Lời giải:
a) Tạo ra chất khí, ví dụ muối cacbonat (CaCO3, Na2CO3, NaHCO3) hoặc dung dịch muối sunfit (Na2SO3) tác dụng với axit (HCl, H2SO4 loãng):
CaCO3 + H2SO4 → CaSO4 + CO2 ↑ + H2O
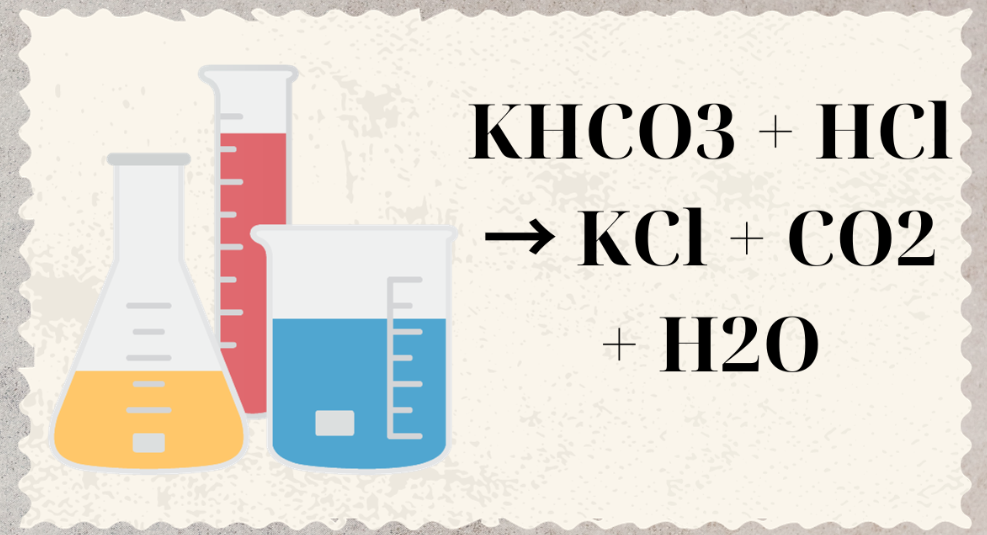
Na2CO3 + 2HCl → 2NaCl + CO2 ↑ + H2O
Na2SO3 + H2SO4 → Na2SO4 + SO2 ↑ + H2O
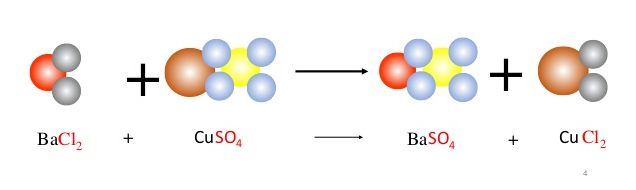
b) Tạo chất kết tủa, ví dụ dung dịch muối (BaCl2, Ba(NO3)2 …) tác dụng với dung dịch H2SO4 tạo ra kết tủa BaSO4.
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
Hoặc những dung dịch muối bari tác dụng với dung dịch muối cacbonat (Na2CO3, K2CO3) tạo ra BaCO3 kết tủa.
Ba(NO3)2 + Na2CO3 → BaCO3 ↓ + 2NaNO3.
Câu 11:
Cho những dung dịch muối sau đây phản ứng với nhau từng đôi một, hãy ghi dấu (x) nếu có phản ứng, dấu (o) nếu không:
| Na2CO3 | KCl | Na2SO4 | NaNO3 | |
| Pb(NO3)2 | ||||
| BaCl2 |
Hãy viết phương trình hóa học ở ô có dấu (x).
Lời giải:
| Na2CO3 | KCl | Na2SO4 | NaNO3 | |
| Pb(NO3)2 | x | x | x | o |
| BaCl2 | x | o | x | o |
Phương trình hóa học của các phản ứng:
Pb(NO3)2 + Na2CO3 → PbCO3 ↓ + 2NaNO3
Pb(NO3)2 + 2KCl → PbCl2 ↓ + 2KNO3
Pb(NO3)2 + Na2SO4 → PbSO4 ↓ + 2NaNO3
BaCl2 + Na2CO3 → BaCO3 ↓ + 2NaCl
BaCl2 + Na2SO4 → BaSO4 ↓ + 2NaCl.
Cách giải bài tập Phản ứng của Ankin với Bạc Nitrat (AgNO3)
– Chỉ có ank-1-in hoặc các chất có liên kết ba đầu mạch mới có phản ứng với AgNO3/NH3.
• Tổng quát:
CnH2n-2 + xAgNO3 + xNH3 → CnH2n-2-xAgx↓ + xNH4NO3.
CxHy + aAgNO3 + aNH3 → CxHy-aAga↓ + aNH4NO3.
Chú ý:
– nankin = n↓ ⇒ m↓ = mankin + 107.n↓.a.
– Khối lượng bình đựng AgNO3/NH3 tăng bằng khối lượng ankin phản ứng.
– Để tái tạo lại ankin ta cho ↓ phản ứng với HCl.
– Anken và ankan không có phản ứng này.
Bài 1: Hỗn hợp khí X gồm etilen và propin. Cho a mol X tác dụng với dung dịch AgNO3 trong NH3, thu được 17,64 gam kết tủa. Mặt khác a mol X phản ứng tối đa với 0,34 mol H2. Giá trị của a là
Lời giải:
nC3H4 = nC3H3Ag = 17,64/147 = 0,12 mol
nC2H4 + 2nC3H4 = nH2 ⇒ nC2H4 = 0,1 mol ⇒ a = nC2H4 + nC3H4 = 0,22 mol
Bài 2: Hỗn hợp X gồm metan, etilen, axetilen. Sục 7 gam X vào nước brom dư thì thấy có 48 gam brom pư. Cho 7 gam trên pư với AgNO3 dư trong NH3 thì thu được 24 gam kết tủa. Tính khối lượng mỗi chất trong X?
Lời giải:
Gọi số mol của metan, etilen, axetilen lần lượt là x, y, z ta có: 16x + 28y + 26z = 7 (1)
Phương trình phản ứng:
C2H4 + Br2 → C2H4Br2
y………y
C2H2 + 2Br2 → C2H2Br4
z………2z
số mol brom phản ứng: nBr2 = 48/160 = 0,3 mol = y + 2z (2)
C2H2 + 2AgNO3 + 2NH3 → C2H2Ag2↓ + 2NH4NO3.
z……………………………….z
Số mol kết tủa: n↓ = 24/240 = 0,1 mol = z (3)
Từ (1), (2), (3) ta có: x = y = z = 0,1 mol
Khối lượng mỗi chất trong X là:
mmetan = 0,1.16 = 1,6 gam; metilen = 0,1.28 = 2,8 gam; maxetilen = 0,1.26 = 2,6 gam
Bài 3: Một hỗn hợp khí (X) gồm 1 ankan, 1 anken và 1 ankin có V =1,792 lít (ở đktc) được chia thành 2 phần bằng nhau:
– Phần 1: Cho qua dung dịch AgNO3/NH3 dư tạo 0,735 g kết tủa và thể tích hỗn hợp giảm 12,5%
– Phần 2: Đốt cháy hoàn toàn rồi hấp thụ sản phẩm cháy vào dung dịch Ca(OH)2 dư thì thấy có 12 gam kết tủa.
Xác định CTPT của các hiđrocacbon và %V các chất trong X biết ankan và anken có cùng số C?
Lời giải:
Số mol ba chất trong X: nX = 0,08 mol⇒ số mol X trong một phần là: n = 0,04 mol
Thể tích hỗn hợp phần 1 giảm 12,5% ⇒ Số mol ankin trong mỗi phần là nankin = 0,04.0,125 = 0,005 mol. Nếu X là axetilen thì khối lượng kết tủa là 1,2 gam (trái với giả thiết)
– Pư với AgNO3/NH3 ta có:
CnH2n-2 + AgNO3 + NH3 → CnH2n-3Ag↓ + NH4NO3.
Mol:0,005 0,005
⇒ 0,005(14n + 105 ) = 0,735 ⇒ n = 3 ⇒ ankin là propin
– Số mol CaCO3 : nCaCO3 = 0,12 mol ⇒ Số Ctb = 3 ⇒ hai chất còn lại là propan và propen.
Bài tập trắc nghiệm
Bài 1: Dẫn V lít (đktc) axetilen qua dung dịch AgNO3/NH3 dư thấy thu được 60 gam kết tủa. Giá trị V là:
A. 5,6 lit B. 11,2 lit C. 2,8 lit D. 10,11 lit
Lời giải:
Đáp án: A
n↓ = 60/240 = 0,25 mol ⇒ naxetilen = 0,25.22,4 = 5,6 lít
Bài 2: Dẫn 10,8 gam but-1-in qua dd AgNO3/NH3 dư, sau phản ứng thu x gam kết tủa. Giá trị của x là
A. 26,8g B. 16,1g C. 53,6g D. 32,2g
Lời giải:
Đáp án: D
nankin = 10,8/54 = 0,2 mol; n↓ = 0,2 mol ⇒ x = 0,2 .161 = 32,2 g
Bài 3: Dẫn 6,72 lít một ankin X qua dung dịch AgNO3/NH3 dư thấy thu được 44,1g kết tủa. CTPT của X là:
A. C2H2. B. C3H4. C. C5H8. D. C4H6.
Lời giải:
Đáp án: B
nX = 0,3 mol ⇒ Mkết tủa = 44,1/0,3 = 147 ⇒ ankin là C3H4.
Bài 4: Dẫn 11,2 lít hh khí X (gồm axetilen và propin) vào dd AgNO3/NH3 dư (các phản ứng xảy ra hoàn toàn), sau phản ứng thu được 92,1 gam kết tủa. % số mol của axetilen trong X là.
A.70% B. 30% C. 60% D. 40%
Lời giải:
Đáp án: D
gọi số mol của axetilen và propin lần lượt là: x và y mol; x + y = 0,5 mol; 240x + 147y = 92,1 ⇒ x = 0,2 và y = 0,3 ; %naxetilen = 0,2.100%/0,5 = 40%
Bài 5: Hỗn hợp X gồm propin và ankin A có tỉ lệ mol 1:1. Lấy 0,3 mol X tác dụng với dd AgNO3/NH3 dư thu được 46,2 gam kết tủa. Vậy A là:
A. Axetilen B. But-2-in. C. But-1-in. D. Pent-1-in.
Lời giải:
Đáp án: C
npropin = nA = 0,15 mol; m↓ = 0,15.147 + m↓A ⇒ m↓A = 46,2 – 22,05 = 22,05 ⇒ M↓ = 22,05/0,15 = 161 ⇒ ankin A là: C4H6 (but-1-in)
Bài 6: Một hỗn hợp gồm C2H2 và đồng đẳng A của axetilen có tỷ lệ mol 1:1. Chia hh thành 2 phần bằng nhau
+ Phần 1 tác dụng vừa đủ với 8,96 lít H2 (đktc) tạo hidrocacbon no.
+ Phần 2 tác dụng với 300ml dd AgNO3 1M/NH3 thu được 40,1g kết tủa. Tên gọi của A là:
A. pent-1-in B. Vinylaxetilen C. but-1-in D. propin
Lời giải:
Đáp án: C
nC2H2 = nA = x; 2x + 2x = 4x = 0,4 mol ⇒ x = 0,1 mol; m↓C2H2 = 0,1.240 = 24 gam ⇒ m↓A = 40,1 – 24 = 16,1 gam ⇒ M↓A = 16,1/0,1 = 161 ⇒ A là but-1-in
Bài 7: Cho 17,92 lít hỗn hợp X gồm 3 hiđrocacbon khí là ankan, anken và ankin lấy theo tỉ lệ mol 1:1:2 lội qua bình đựng dd AgNO3/NH3 lấy dư thu được 96 gam kết tủa và hỗn hợp khí Y còn lại. Đốt cháy hoàn toàn hỗn hợp Y thu được 13,44 lít CO2. Biết thể tích đo ở đktc. Khối lượng của X là
A. 19,2 gam. B. 1,92 gam. C. 3,84 gam. D. 38,4 gam.
Lời giải:
Đáp án: A
nX = 0,8 mol; nankan = nanken = 0,2 mol; nankin = 0,4 mol; M↓ankin = 96/0,4 = 240 ⇒ ankin là C2H2; nCO2 = 0,6 = 0,2n + 0,2m ⇒ n = 1 và m = 2 ⇒ ankan và ankin là: CH4 và C2H4
⇒ mX = 0,2.16 + 0,2.28 + 0,4.26 = 19,2 g
Bài 8: Đốt cháy hoàn toàn m gam ankin A bằng O2 vừa đủ thu được 22,4 lít CO2 (đktc). Mặt khác, dẫn m gam A qua dd AgNO3/NH3 dư thấy có 35 gam kết tủa màu vàng nhạt. CTPT của A là.
A. C7H12 B. C8H14 C. C5H8 D. C6H10
Lời giải:
Đáp án: C
CTPT ankin A: CnH2n-2 ; nA = 1/n; M↓A = 35n ⇒ n =5, M = 175 ⇒ A là C5H8